Grundlegende chemische Reaktionen wurden oft nach ihren Entdeckern/Entwicklern benannt. Sie stellen ein Fundament in der Organischen Chemie dar und helfen bei der Aufstellung von komplizierten Synthesen. Als Auftragshersteller von "small organic molecules" und Polymeren beschäftigt sich ChemCon natürlich mit der Entwicklung von Synthesen und dem Überführen von Synthesen aus dem Labor in einen größeren Maßstab (Upscaling). Somit sind diese Namensreaktionen, die alle bereits in ChemCon Laboren angewendet wurden, eine der chemischen Grundlagen für unsere synthetische Arbeit.
Hier ist eine Liste mit Namensreaktionen gegeben, die wöchentlich erweitert wird. So entwickelt sich ein Nachschlagwerk, das nicht nur Studierenden helfen soll.
Namensreaktionen
Osman Achmatowicz wurde am 16. April 1899 in Belarus geboren. Seinen Schulabschluss inklusive Abitur machte er in Sankt Petersburg. Anschließend studierte Achmatowicz an der Stefan-Bathory-Universität in Wilna wo er auch der ältesten polnischen Studentenverbindung „Konvent Polonia“ angehörte.
Später wurde er sowohl zum Mitglied der Polnischen Akademie der Gelehrsamkeit als auch zum Mitglied der Warschauer Wissenschaftsgesellschaft gewählt. Im Jahr 1960 erhielt er von der Technischen Hochschule Łódź die Ehrendoktorwürde.
Die im Jahr 1971 entwickelte Achmatowicz-Reaktion wurde nach ihm benannt.
Bei der Acyloin-Kondensation reagieren zwei Ester unter Bildung eines Acyloins. Die Reste R1 und R2 sind Organylreste.
Mechanistisch reagiert der 1. Ester mit Natrium, welches die Reaktion ermöglicht, und bildet ein radikalisches Anion. Dieses Anion reagiert mit dem radikalischen Anion, das aus dem anderen Ester gebildet wurde zu einem Dianion. Durch Abspaltung von zwei Alkoholatresten (R2O-) entsteht ein Diketon, das mit überschüssigem Natrium zu einem Dianion reduziert wird. Dieses Dianion wird dann bei wässriger Aufarbeitung zum α-Hydroxyketon, Acyloin, hydrolysiert.
Charles Adolphe Wurtz und Alexander Porfyrech Borodin enteckten Ende des 19. Jahrhundert unabhängig voneinander diesen Reaktionstyp.
Charles Adolphe Wurtz war ein französicher Chemiker und Arzt. Geboren wurde er 1817 in Straßburg. Über ein Studium der Medizin bei dem er sich sehr für die klinische Chemie interessierte, ging er für ein Jahr zu Justus Liebig nach Giessen. Anschließend kehrte er nach Paris zurück. Wurtz beschäftigte sich mit der organischen Chemie, insbesondere mit organischen Stickstoffverbindungen. An der berühmten Sorbonne war Wurtz der erste Lehrstuhlinhaber für organische Chemie. Die Wurtz-Fittig-Synthese ist eine weitere Namensreaktion, bei der Charles Adolphe Wurtz mitarbeitete.
Alexander Porfyrech Borodin war ein russischer Komponist, Professor der organischen Chemie und Mediziner. Geboren wurde Bordi Anfang des 19. Jahrhunderts in St. Petersburg. Musikalische Begabung und eine gute musische Erziehung ließ ihn mehrere Instrumente lernen. 1850 begann er sein Studium der Medizin und 1859 das der Chemie. Bereits mit 29 Jahren erhielt Borodin eine Professur für organische Chemie. Auch auf dem Gebiet der Fluorverbindungen forschte Borodin.
Rolf Appel wurde 1921 in Hamburg geboren und studierte an der Martin-Luther-Universität Halle-Wittenberg Chemie. Promoviert wurde er 1951 von der Chemikerin Margot-Becke-Goehring. Nach dem Studium übernahm er 1962 an der Universität Bonn einen Chemie-Lehrstuhl.
Eine große Ehrung wurde ihm zuteil, als er 1986 als Auszeichnung die Liebig-Denkmünze erhalten hatte. Bekannt geworden ist er für die nach ihm benannte Reaktion.
Friedrich Asinger wurde 1907 in Niederösterreich geboren. Nach seinem Abitur in Krems an der Donau im Jahr 1924 begann er sein Chemiestudium an der TH Wien. 1932 promovierte er mit einer Arbeit über den Einfluss von Substituenten auf die Verseifungsgeschwindigkeit von Benzalchlorid.
Nach verschiedenen Industrieanstellungen habilitierte sich Asinger 1943 an der Universität Graz und wurde 1944 Dozent an der Martin-Luther-Universität Halle-Wittenberg. Aufgrund von Verbindungen zur NSDAP verlor er diese Position nach Ende des Zweiten Weltkriegs. 1946 wurde er mit anderen Wissenschaftlern in die Sowjetunion verschleppt, wo er als Arbeitsgruppenleiter an der Entwicklung von Raketentreibstoffen beteiligt war und Synthesewege zu Schwefel- und Stickstoff-haltigen Heterocyclen entdeckte.
Ab 1954 kehrte Asinger nach Deutschland zurück und folgte 1957 einem Ruf an die Martin-Luther-Universität Halle (Saale) sowie später an die TU Dresden. In dieser Zeit ermutigte er unter anderem Becker dazu, das Organikum zu schreiben.
Ab 1959 leitete Asinger das Institut für Technische Chemie und Petrochemie an der RWTH Aachen. Hier entwickelte er die Stickstoff-Schwefel-Heterocyclen-Chemie weiter, die heute als Asinger-Chemie bekannt ist. Ein Beispiel dafür ist die dreizehnstufige Synthese von D-Penicillamin, deren Ausgangsreaktion die Asinger-Synthese ist.
Durch eine Asinger-Synthese-analoge Reaktion können auch 3-Oxazoline hergestellt werden. Die bedeutenderen Oxazoline sind jedoch die 2-Oxazoline, die durch kationische Ringöffnungspolymerisation polymerisiert werden können. Je nach Kettenlänge, Vernetzungsgrad und angefügten funktionellen Gruppen können diese unterschiedlichste Funktionalitäten aufweisen. Die Polymere aus 2-Oxazolin werden als Polyoxazoline bezeichnet.
ChemCon beschäftigt sich seit vielen Jahren mit der Synthese dieser Polymeren und ist in der Lage, sie nach den Wünschen der Kunden unter GMP-Bedingungen herzustellen. Das Unternehmen verfügt über Synthese- und Analytikexperten sowie langjährige Erfahrung im Bereich GMP und GMP-Dokumentation, die durch Inspektionen der FDA und deutscher Behörden belegt ist.
Alexander Roberts Atherton war ein angesehener Chemiker, dessen Beiträge auf dem Gebiet der Chemie bleibende Spuren hinterlassen haben. Geboren 1911 in Cambridge, England, war Athertons frühes Leben von einer tiefen Neugier auf die Natur geprägt. Diese Neugier führte ihn zu einer Karriere in der Chemie, in der er bedeutende Fortschritte erzielen sollte.
Athertons akademische Laufbahn begann an der Universität Cambridge, wo sich seine Leidenschaft für die Chemie schnell zeigte. Seine Hingabe zum Studium brachte ihm zahlreiche Auszeichnungen ein, und er schloss sein Chemiestudium als Jahrgangsbester ab. Nach seinem Bachelor-Abschluss setzte Atherton sein Studium an der Goethe-Universität Frankfurt fort, wo er in organischen Reaktionsmechanismen promovierte. Nach dieser bemerkenswerten Leistung erwarb er einen zweiten Doktortitel an der Universität Oxford, wo er sich auf die Entwicklung neuer Synthesemethoden konzentrierte.
Eines von Athertons bemerkenswertesten Errungenschaften war die Entwicklung der Atherton-Todd-Reaktion, einer neuartigen Methode zur Umwandlung von Dialkylphosphiten in Dialkylphosphate. Diese Reaktion, bei der Trichlormethan und eine Base verwendet werden, ist zu einem grundlegenden Prozess in der organischen Synthese geworden. Die Vielseitigkeit und Effizienz der Atherton-Todd-Reaktion haben sie zu einem wertvollen Werkzeug für Chemiker weltweit gemacht, und sie wird sowohl in der akademischen Forschung als auch in industriellen Anwendungen häufig genutzt.
Athertons Beiträge zur Chemie wurden im Laufe seiner Karriere mit zahlreichen Ehrungen und Auszeichnungen gewürdigt. 1965 erhielt er den Nobelpreis für Chemie für seine bahnbrechenden Arbeiten zu Nukleotiden und Nukleotid-Coenzymen. Das Nobelkomitee hob seinen innovativen Ansatz und die breite Anwendbarkeit seiner Forschung als wesentliche Fortschritte auf diesem Gebiet hervor. Neben dem Nobelpreis erhielt Atherton mehrere andere prestigeträchtige Auszeichnungen, darunter die Copley-Medaille und die Priestley-Medaille, die beide zu den höchsten Ehrungen im Bereich der Chemie zählen.
Athertons Einfluss reichte über seine Forschung hinaus. Er war ein engagierter Lehrer und Mentor für zahllose Studenten und junge Wissenschaftler, die später eigene Beiträge zum Fachgebiet leisten sollten. Sein Engagement für die Lehre und seine Fähigkeit, andere zu inspirieren, machten ihn zu einer beliebten Persönlichkeit in der akademischen Gemeinschaft.
In seinen späteren Jahren blieb Atherton in der wissenschaftlichen Gemeinschaft aktiv, besuchte regelmäßig Konferenzen und arbeitete mit anderen führenden Chemikern zusammen. Seine Arbeiten wurden in zahlreichen wissenschaftlichen Zeitschriften veröffentlicht und seine Beiträge wurden weltweit von Forschern vielfach zitiert.
Das Vermächtnis von Alexander Roberts Atherton ist eines von Innovation, Hingabe und Exzellenz. Seine Errungenschaften in der Chemie haben das Fachgebiet tiefgreifend beeinflusst und sein Einfluss wird noch für viele Generationen spürbar sein. Sein Leben dient als Inspiration für angehende Chemiker und erinnert an das unglaubliche Potenzial wissenschaftlicher Entdeckungen.
Adolf von Baeyer wurde im Oktober 1835 als fünftes von sieben Kindern in Berlin geboren. Nachdem er am Friedrich-Wilhelms-Gymnasium seinen Schulabschluss gemacht hatte, studierte er Mathematik und Physik an der Friedrich-Wilhelms-Universität in Berlin, sowie Chemie an der Ruprecht-Karls-Universität in Heidelberg.
Adolf war Gründungsmitglied der „Deutschen Chemischen Gesellschaft“ zu Berlin, die die Fachzeitschrift „Berichte der Deutschen Chemischen Gesellschaft“ veröffentlichten.
An seinem 50. Geburtstag wurde er von König Ludwig II. von Bayern in den erblichen Adelsstand erhoben und erhielt den Titel „von“.
Die Baeyer-Indol-Synthese wurde im Jahr 1869 von Adolf von Baeyer und Adolphe Emmerling entdeckt.
1905 erhielt von Baeyer den Nobel Preis für seine Arbeiten zu organischen Farbstoffen.
Victor Villiger wurde im Jahr 1868 am Zuger See in der Schweiz geboren. Nach seinem Schulabschluss studierte Villiger Chemie an der Universität Genf, bevor er zum Militärdienst eingezogen wurde.
1890 kam er an die Universität München, wo er später mit seiner Arbeit über die Hexahydro-isophthalsäure promovierte. In dieser Zeit lernte er auch seinen Mentor Adolf von Baeyer kennen. Die beiden arbeiteten 11 Jahre zusammen und haben zwischen 1899 und 1900 gemeinsam die Baeyer-Villiger-Oxidation entwickelt.
Adolf von Baeyer wurde im Oktober 1835 als fünftes von sieben Kindern in Berlin geboren. Nachdem er am Friedrich-Wilhelms-Gymnasium seinen Schulabschluss gemacht hatte, studierte er Mathematik und Physik an der Friedrich-Wilhelms-Universität in Berlin, sowie Chemie an der Ruprecht-Karls-Universität in Heidelberg.
Adolf war Gründungsmitglied der „Deutschen Chemischen Gesellschaft“ zu Berlin, die die Fachzeitschrift „Berichte der Deutschen Chemischen Gesellschaft“ veröffentlichten.
An seinem 50. Geburtstag wurde er von König Ludwig II. von Bayern in den erblichen Adelsstand erhoben und erhielt den Titel „von“.
Günther Schiemann wurde 1899 in Breslau geboren. Er besuchte die Universität Breslau und promovierte dort im Jahr 1925 zum Dr. phil. mit einer Arbeit, die den Titel "Über den Mechanismus der Oxidation der Harnsäure" trug. Anschließend war er bis 1926 als Volontärassistent an der ETH Zürich bei Hermann Staudinger tätig. In den Jahren 1926 und 1935 arbeitete Schiemann als Assistent und Oberassistent an der Technischen Hochschule Hannover, wo er ab 1929 auch als Privatdozent lehrte. Die Balz-Schiemann Synthese gelang ihm erstmals im Jahr 1927. Aufgrund seiner jüdischen Abstammung wurde ihm 1935 seine Anstellung und 1937 auch seine Dozentur gekündigt. Zwischen 1935 und 1950 arbeitete Schiemann in der Privatwirtschaft. Im Jahr 1946 wurde er nebenberuflicher Dozent in Hannover und im Jahr 1950 Professor an der Universität Istanbul, wo er das "Sinai Kimya Institut" leitete. Im Jahr 1956 kehrte er als Professor nach Hannover zurück und leitete dort das Institut für Technische Chemie.
Fast 20% der 200 meistverkauften Arzneiwirkstoffe des Jahres 2018 enthielten mindestens ein Arylfluorid oder ein Derivat davon.
François Antoine Philippe Barbier, ein Name, der außerhalb der Chemiekreise vielleicht nicht allzu bekannt ist, nimmt einen zentralen Platz in den Annalen wissenschaftlicher Innovationen ein. Geboren in der Strenge des 19. Jahrhunderts in Frankreich, war Barbiers Weg in die Welt der Chemie von einer unersättlichen Neugier und einer unerschütterlichen Hingabe an die Erforschung geprägt. Seine Arbeit legte die Grundsteine für zukünftige Entdeckungen, überschritt die Grenzen seiner Zeit und nährte Talente, die die Welt der Wissenschaft weiter revolutionieren sollten.
Barbiers akademische Reise begann mit einer soliden Ausbildung in den Naturwissenschaften, wo er bereits in jungen Jahren bemerkenswerte Fähigkeiten zeigte. Seine Leidenschaft für chemische Forschung katapultierte ihn durch die Reihen der Akademie und gipfelte in einer herausragenden Karriere als Chemiker. Seine wissenschaftlichen Bestrebungen waren von einem Pioniergeist geprägt, der darauf bedacht war, die unerforschten Gebiete chemischer Reaktionen und ihrer vielfältigen Anwendungen zu erkunden.
Unter Barbiers zahlreichen Beiträgen zur Chemie sticht die Barbier-Reaktion als Zeugnis seines Einfallsreichtums hervor. Dieser bahnbrechende Syntheseprozess, der die Erstellung von sekundären oder tertiären Alkoholen aus halogenierten Verbindungen ermöglicht, eröffnete neue Wege in der Synthese komplexer organischer Moleküle. Die Eleganz der Reaktion liegt in ihrer Einfachheit und Effizienz, Eigenschaften, die sie zu einem Grundpfeiler in organischen Syntheselaboren weltweit gemacht haben.
Vielleicht ist eines von Barbiers dauerhaftesten Vermächtnissen sein Einfluss auf seine Studenten, unter denen Victor Grignard war, ein Name, der mit dem Nobelpreis für Chemie gleichgesetzt wird. Grignard, der 1912 den Nobelpreis erhielt, profitierte direkt von Barbiers Mentorship. Die Grignard-Reaktion, eine Weiterentwicklung von Barbiers eigener Forschung, erweiterte das Werkzeugset der Chemiker weiter, indem sie die Bildung von Kohlenstoff-Kohlenstoff-Bindungen auf eine zuvor als unpraktisch angesehene Weise ermöglichte.
Die Beziehung zwischen Barbier und Grignard veranschaulicht den tiefgreifenden Einfluss, den ein Mentor auf die Richtung wissenschaftlicher Entdeckungen haben kann. Unter Barbiers Anleitung verfeinerte Grignard nicht nur seine Fähigkeiten, sondern entwickelte auch die grundlegenden Ideen, die zu seiner preisgekrönten Arbeit führen würden. Diese Mentor-Mentee-Dynamik unterstreicht die Bedeutung akademischer Abstammung in der Weitergabe von Wissen und Innovation.
Barbiers Leben, gefüllt mit akademischen Errungenschaften und wissenschaftlichen Durchbrüchen, leuchtet den Weg für zukünftige Generationen von Chemikern. Sein Vermächtnis, gekennzeichnet durch die Barbier-Reaktion und seine Rolle in der Förderung von Nobelpreisträgern, hallt weiterhin in der wissenschaftlichen Gemeinschaft nach. Durch seine Beiträge hat Barbier nicht nur das Feld der Chemie vorangebracht, sondern auch den dauerhaften Wert von Mentorship und den gemeinschaftlichen Geist wissenschaftlicher Untersuchungen demonstriert.
Wenn wir auf die beeindruckende Karriere von François Antoine Philippe Barbier zurückblicken, wird deutlich, dass seine Arbeit nicht nur um die Moleküle und Reaktionen kreiste, die seinen Namen tragen, sondern auch um die Förderung einer Kultur der Neugier und Ausdauer. Sein Erbe, verankert in den Annalen der Chemie, dient als Leuchtfeuer für angehende Wissenschaftler und erinnert uns an die Kraft der Erkundung und die endlosen Möglichkeiten, die jenen warten, die es wagen zu hinterfragen und zu entdecken.
Heinrich Wieland, eine herausragende Persönlichkeit der organischen Chemie, hat mit seinen bahnbrechenden Forschungen und seinem prägenden Einfluss als Lehrer ein unvergängliches Vermächtnis hinterlassen. Geboren am 4. Juni 1877 in Pforzheim, wuchs Wieland in einer Familie auf, die eng mit der chemischen Industrie verbunden war. Diese frühe Prägung weckte vermutlich seine Leidenschaft für die Chemie, die er mit unermüdlicher Neugier und außergewöhnlichem Talent verfolgte.
Nach seinem Studium an der Universität München begann Wieland seine wissenschaftliche Laufbahn mit einem Fokus auf organische Verbindungen und deren komplexe Reaktionsmechanismen. Bereits früh widmete er sich der Chemie der Gallensäuren und Stickstoffverbindungen – Themen, die ihn zeitlebens begleiten und zu seinen größten Erfolgen führen sollten. Wielands systematischer Ansatz, chemische Prozesse zu entschlüsseln, hob ihn als präzisen und visionären Forscher hervor.
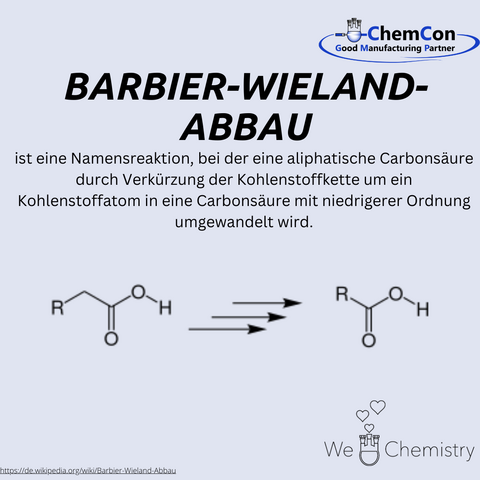
Eines seiner bedeutendsten Vermächtnisse ist die nach ihm benannte Barbier-Wieland-Abbau-Reaktion. Diese elegante Methode ermöglicht die Verkürzung von Kohlenstoffketten in aliphatischen Carbonsäuren um ein Kohlenstoffatom. Die Reaktion wurde schnell zu einem unverzichtbaren Werkzeug in der Strukturaufklärung organischer Verbindungen. Sie zeigt Wielands außergewöhnliche Fähigkeit, praktische Methoden zu entwickeln, die die Möglichkeiten der Chemie erheblich erweiterten.
Seine Zeit als Professor an der Universität Freiburg von 1913 bis 1921 war sowohl für ihn als auch für die Universität von großer Bedeutung. Hier entwickelte er sich zu einem wegweisenden Mentor und inspirierenden Leiter, der eine Atmosphäre intellektueller Neugierde und wissenschaftlicher Strenge schuf. Wielands Vorlesungen waren für ihre Klarheit und Tiefe bekannt und machten ihn bei Studierenden und Kollegen gleichermaßen beliebt. Unter seiner Leitung entwickelte sich Freiburg zu einem Zentrum innovativer chemischer Forschung. Er zog zahlreiche talentierte Nachwuchswissenschaftler an, die von seiner Fähigkeit profitierten, grundlegende Prinzipien mit praxisorientierten Anwendungen zu verknüpfen. Diese Jahre waren geprägt von einem lebhaften Austausch von Ideen, der viele seiner Schüler dazu befähigte, selbst bedeutsame Beiträge zur Chemie zu leisten.
1927 wurde Heinrich Wieland für seine herausragenden wissenschaftlichen Leistungen mit dem Nobelpreis für Chemie ausgezeichnet. Er erhielt diese höchste wissenschaftliche Ehre für seine wegweisenden Forschungen zur Struktur und Funktion der Gallensäuren. Wielands Arbeiten offenbarten die komplexe Biochemie dieser Substanzen und klärten ihre Rolle bei Verdauungs- und Stoffwechselprozessen auf. Das Nobelkomitee würdigte seine Beiträge als entscheidend für das Verständnis von Naturstoffen – einem Bereich, der tiefgreifende Auswirkungen auf Medizin und Biologie hat. Die Verleihung des Nobelpreises bestätigte nicht nur Wielands Stellung als einer der größten Chemiker seiner Zeit, sondern unterstrich auch die Bedeutung seiner sorgfältigen und innovativen Forschung.
Neben seinen wissenschaftlichen Erfolgen lag Wieland auch die Förderung von Integrität und sozialer Verantwortung in der Wissenschaft am Herzen. Bis zum Ende seiner Karriere blieb er eine treibende Kraft in der chemischen Forschung und hinterließ ein Vermächtnis, das weit über seine Publikationen und Entdeckungen hinausgeht.
Heinrich Wieland verstarb am 5. August 1957 und hinterließ ein Erbe, das bis heute Generationen von Chemikern inspiriert. Besonders seine Zeit in Freiburg und die Auszeichnung mit dem Nobelpreis stehen exemplarisch für seinen Beitrag zur Wissenschaft. Mit seinen Arbeiten erweiterte Heinrich Wieland nicht nur die Grenzen der Chemie, sondern setzte auch Maßstäbe dafür, welchen bleibenden Einfluss ein einzelner Mensch auf die wissenschaftliche Welt haben kann.
Derek H.R. Barton war ein britischer Chemiker, der 1969 den Nobelpreis für Chemie erhielt. Er wurde am 8. September 1918 in Gravesend, Kent, geboren und studierte ab 1938 am Imperial College der University of London. Nach Abschluss seines Studiums arbeitete er für zwei Jahre als Chemiker in einem Regierungsprogramm. Danach wechselte er zum Imperial College nach Birmingham, wo er für zwei Jahre als Lehrbeauftragter tätig war. Von 1946 bis 1949 arbeitete er als wissenschaftlicher Mitarbeiter im Imperial Chemical Industries (ICI). Von entscheidender Bedeutung für seinen weiteren beruflichen Entwicklungsweg war die 1949 beginnende Gastdozentur an der Harvard University (USA) in der Abteilung Naturstoffchemie. Hier lernte er den US-amerikanischen Wissenschaftler und Chemiker Robert B. Woodward kennen. Beide verband ab diesem Zeitpunkt eine lebenslange wissenschaftliche Zusammenarbeit und enge Freundschaft. Damit begann seine bahnbrechende wissenschaftliche Arbeit über die Konformationsanalyse.
Barton arbeitete auch mit dem Unternehmen Schering-Plough zusammen und bearbeitete an seinem Forschungsinstitut für Medizin und Chemie in Cambridge das Thema “Aldosteron”. Dabei entdeckte er, was heute als Barton-Reaktion bekannt ist, einen photochemischen Prozess, der eine relativ einfache Methode zur Synthese von Aldosteron ermöglicht. Das war ein großer Erfolg seiner Forschungsarbeit. Daraus entwickelten sich fast 40 Jahre enge Praxisbeziehungen zwischen der medizinischen Forschung und der Pharmaindustrie.
Die Barton-Decarboxylierung ist eine Namensreaktion der organischen Chemie. Mit ihrer Hilfe können organische Reste von Carbonsäurechloriden oder Carbonsäuren abgespalten werden.
Bartons Einfluss auf die heutige Pharmazie ist enorm. Seine Forschungsarbeit hat dazu beigetragen, dass die Synthese von Aldosteron und anderen Steroiden heute einfacher und effizienter ist. Seine bahnbrechenden Arbeiten zur Konformationsanalyse haben auch die Struktur und Synthese von Steroiden revolutioniert. Seine Entdeckungen haben die pharmazeutische Forschung und Entwicklung vorangetrieben und die Grundlage für viele wichtige Medikamente gelegt.
Antoine Béchamp wurde 1816 in Frankreich geboren, ging aber als Siebenjähriger mit seinem Onkel nach Bukarest. 1831 fing er dort eine Apothekerlehre an, die er aber erst einige Jahre später in Frankreich beendete. Nachdem er seine eigene Apotheke gegründet hatte, arbeitete er an der Apothekerschule im Bereich Chemie, Physik und Toxikologie. In dieser Zeit lernte er den Chemie-Professor Louis Pasteur kennen, welchem er seine Doktorarbeit in Chemie widmete. Auf der Grundlage dieser Arbeit entwickelte er 1852 seine Béchamp-Reduktion, welche zum Aufstieg der Farbenindustrie beitrug.
Ernst Otto Beckmann (1853–1923) war ein deutscher Chemiker, dessen bahnbrechende Beiträge die moderne organische und physikalische Chemie maßgeblich prägten. Von seiner akademischen Laufbahn über seine innovativen Methoden bis hin zur berühmten Beckmann-Umlagerung – sein Vermächtnis bleibt bis heute von großer Bedeutung, insbesondere bei der Herstellung essenzieller Medikamente wie Paracetamol.
Geboren am 4. Mai 1853 in Solingen, zeigte Beckmann früh Interesse an den Naturwissenschaften. Er begann seine Ausbildung in der Pharmazie und schloss sein erstes Studium 1875 ab. Doch sein Wissensdurst und sein Ehrgeiz führten ihn bald weiter in die Chemie, die er an der Universität Leipzig unter dem berühmten Chemiker Hermann Kolbe vertiefte. Kolbe, einer der Begründer der strukturellen organischen Chemie, prägte Beckmanns wissenschaftliches Denken und dessen spätere Errungenschaften maßgeblich. 1878 promovierte Beckmann mit einer Arbeit über organische Synthese und die Chemie von Aminen. Seine anschließenden Forschungsjahre konzentrierten sich auf die strukturellen Umwandlungen organischer Verbindungen und ebneten den Weg für seine bedeutendste Entdeckung.
1886 beschrieb Beckmann eine chemische Reaktion, die später seinen Namen tragen sollte: die Beckmann-Umlagerung. Diese Reaktion wandelt Ketoxime oder Aldoxime unter Säurekatalyse in Carbonsäureamide um. Dabei entsteht zunächst eine Zwischenstufe, gefolgt von einer Wanderung einer benachbarten Substituentengruppe, die schließlich das Carbonsäureamid als Endprodukt liefert. Dank ihrer Vielseitigkeit, einfache Verbindungen in wertvolle Zwischen- und Endprodukte umzuwandeln, wurde diese Reaktion rasch zu einem unverzichtbaren Werkzeug in der organischen Synthese – sowohl in der Grundlagenforschung als auch in industriellen Anwendungen.
Die Beckmann-Umlagerung ist auch heute noch von großer Relevanz, insbesondere in der pharmazeutischen Industrie. Ein herausragendes Beispiel ist ihre Rolle bei der industriellen Herstellung von Paracetamol (Acetaminophen), einem der weltweit meistverwendeten Schmerz- und Fiebermittel. Paracetamol steht auf der Liste der unentbehrlichen Arzneimittel der Weltgesundheitsorganisation (WHO), da es eine Schlüsselrolle in der medizinischen Versorgung einnimmt. Die Beckmann-Umlagerung ermöglicht eine effiziente und großtechnische Umwandlung chemischer Vorstufen in die Carbonsäureamid-Struktur, die das Rückgrat dieses lebenswichtigen Medikaments bildet. Dies verdeutlicht eindrucksvoll, wie bedeutend Beckmanns Entdeckung auch heute noch ist.
Neben seinen Arbeiten in der organischen Chemie leistete Beckmann auch wesentliche Beiträge zur physikalischen Chemie. So entwickelte er das Beckmann-Kryoskop, ein Gerät zur Messung der Gefrierpunktserniedrigung von Lösungen. Diese Innovation bot eine äußerst präzise Methode zur Bestimmung von Molekulargewichten und wurde schnell zu einem Standardwerkzeug in physikalisch-chemischen Laboren. Durch die Nutzung des Prinzips, dass der Gefrierpunkt eines Lösungsmittels durch gelöste Stoffe herabgesetzt wird, ermöglichte Beckmanns Konstruktion exakte Messungen selbst in kleinsten Temperaturbereichen – ein weiterer Beweis seines experimentellen Einfallsreichtums.
Beckmanns Erfolg war eng mit seinem Lehrer Hermann Kolbe verbunden, einem der führenden Chemiker des 19. Jahrhunderts. Kolbes Fokus auf systematische Strukturanalysen und rigorose experimentelle Methoden prägte Beckmanns Herangehensweise an die Forschung nachhaltig. Beckmann trug dieses Erbe weiter, indem er selbst Studierende ausbildete und die Chemie durch seine innovativen Techniken und Entdeckungen voranbrachte.
Beckmanns Beiträge sind auch in der heutigen Zeit allgegenwärtig. Die Beckmann-Umlagerung, mit ihrer andauernden Bedeutung für die Synthese von Pharmazeutika und Feinchemikalien, unterstreicht die zeitlose Relevanz seiner Arbeit. Paracetamol, eines der weltweit am häufigsten eingesetzten Medikamente, ist ein essenzieller Bestandteil der modernen Gesundheitsversorgung. Es lindert täglich Schmerzen und Fieber bei Millionen von Menschen und steht sinnbildlich für den nachhaltigen Einfluss von Beckmanns Forschung auf die öffentliche Gesundheit.
Ernst Otto Beckmann war nicht nur ein Chemiker, sondern ein Innovator, dessen Entdeckungen die Grenzen zwischen organischer und physikalischer Chemie überbrückten. Von der wegweisenden Beckmann-Umlagerung bis zum Kryoskop steht sein Werk beispielhaft für den nachhaltigen Einfluss wissenschaftlicher Neugierde. In einer Welt, die weiterhin auf seine Entdeckungen angewiesen ist, erinnert Beckmanns Vermächtnis daran, wie Chemie unsere Gesellschaft und unser Leben formen kann.
Pietro Biginelli, ein italienischer Chemiker aus dem späten 19. Jahrhundert, ist vor allem für die Entdeckung der Biginelli-Reaktion bekannt, einer wichtigen Mehrkomponentenreaktion, die in der modernen pharmazeutischen Chemie eine bedeutende Rolle spielt. Obwohl er zu Lebzeiten nicht besonders berühmt war, hat Biginellis Arbeit einen bleibenden Einfluss auf die organische Synthesechemie und die Herstellung von aktiven pharmazeutischen Wirkstoffen (APIs) hinterlassen.
Biginelli wurde 1860 geboren und verfolgte seine Leidenschaft für die Chemie an der Universität Florenz, wo er den Großteil seiner bahnbrechenden Forschung betrieb. Über sein frühes Leben ist wenig bekannt, doch seine akademische Laufbahn führte ihn zu einem wichtigen Beitrag in der chemischen Synthese, bei dem er Methoden zur Vereinfachung der Bildung komplexer organischer Verbindungen entwickelte. Seine bekannteste Entdeckung, die Biginelli-Reaktion, entstand aus dem Bestreben, mehrstufige Prozesse in einen effizienteren und einfacher durchzuführenden Einzelschritt zu verwandeln.
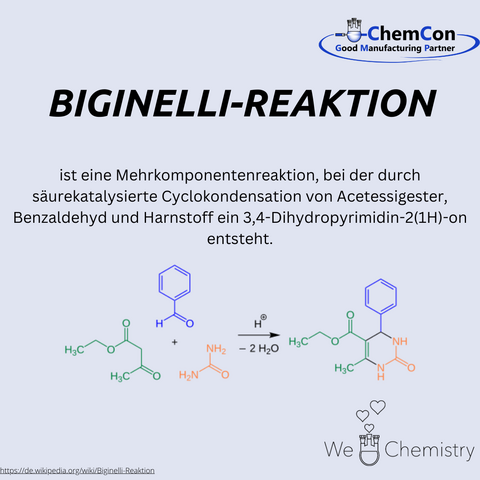
Im Jahr 1891 entdeckte Biginelli eine Reaktion, die später seinen Namen tragen sollte. Die Biginelli-Reaktion ist eine Mehrkomponenten-Cyclokondensation, die die Synthese von 3,4-Dihydropyrimidin-2(1H)-onen (DHPMs) aus einfachen Ausgangsstoffen wie Acetessigester, Benzaldehyd und Harnstoff ermöglicht. Der säurekatalysierte Prozess war für seine Einfachheit und Effizienz bemerkenswert. Zu jener Zeit waren solche One-Pot-Reaktionen besonders begehrt, da sie die Anzahl der Schritte zur Herstellung wertvoller Verbindungen reduzierten und den Prozess weniger arbeitsintensiv und kostengünstiger machten.
Heute spielt die Biginelli-Reaktion eine entscheidende Rolle bei der Synthese pharmazeutischer Verbindungen, insbesondere von APIs. Der 3,4-Dihydropyrimidin-2(1H)-on-Kern ist ein häufig verwendetes Gerüst in biologisch aktiven Molekülen, was ihn zu einem wichtigen Baustein in Arzneimitteln mit entzündungshemmenden, antiviralen und krebshemmenden Eigenschaften macht. Die Anpassungsfähigkeit der Reaktion, die eine Vielzahl von Substituenten zulässt, macht sie in der medizinischen Chemie äußerst wertvoll für die Entwicklung neuer therapeutischer Wirkstoffe.
Die Reaktion wird weit verbreitet in der Produktion von Calciumkanalblockern, antiviralen Medikamenten und anderen wichtigen APIs eingesetzt. Sie bleibt ein unverzichtbares Werkzeug in der Wirkstoffforschung und -entwicklung und bildet aufgrund ihrer Effizienz und Vielseitigkeit eine Grundlage für die Entwicklung neuer pharmazeutischer Verbindungen.
Obwohl Pietro Biginellis Name vielleicht nicht so bekannt ist wie der seiner Zeitgenossen, hat sein Beitrag zur Chemie einen bleibenden Eindruck in der modernen Wissenschaft hinterlassen. Die Biginelli-Reaktion erleichtert nach wie vor die effiziente Synthese komplexer Moleküle und spielt eine wesentliche Rolle bei der Entwicklung lebensrettender Medikamente. Seine Entdeckung zeigt, wie Neugier-getriebene Forschung tiefgreifende und dauerhafte Auswirkungen auf Industrien wie die Pharmazeutik haben kann, wo Innovation ständig im Wandel ist. Biginellis Arbeit erinnert daran, dass selbst bescheidene Entdeckungen zu bedeutenden Fortschritten führen können und grundlegende Werkzeuge für kritische moderne Anwendungen im Gesundheitswesen und darüber hinaus liefern.
Arthur Birch wurde 1915 in Sydney/Australien geboren. Er studierte an der Universität von Sydney, wo er 1937 den Bachelor of Science und 1938 den Master of Science erwarb.1940 wurde er an der Universität von Oxford/UK promoviert. 1952 übernahm Birch eine Professur für Organische Chemie an der Universität von Sydney. 1958 wechselte er erneut nach UK und übernahm eine Professur an der Universität von Manchester. Von 1967 bis 1980 war Birch Dekan an der Australian National University of Canberra.
Durch die Birch'sche Reduktion konnte erstmalig ein Steroid chemisch synthetisiert werden, was für die Pharmazeutische Industrie bis heute von großer Bedeutung ist.
Edmund Napieralski ist ein bedeutender Name in der Chemie, insbesondere aufgrund seiner Beiträge zur organischen Synthese. Obwohl über sein frühes Leben und seinen akademischen Werdegang wenig bekannt ist, bleibt seine Arbeit, insbesondere die Mitentdeckung der Bischler-Napieralski-Reaktion, ein Meilenstein in der heterocyclischen Chemie.
In Zusammenarbeit mit dem Chemiker Alfred Bischler entwickelte Napieralski eine Reaktion, die heute als Bischler-Napieralski-Reaktion bekannt ist. Diese Reaktion spielt eine zentrale Rolle bei der Synthese von Isochinolinen, einer Klasse von Verbindungen, die für die Herstellung von Alkaloiden und pharmazeutischen Wirkstoffen von großer Bedeutung sind. Die Bischler-Napieralski-Reaktion beinhaltet die Cyclodehydratisierung eines β-Phenylethylamids mithilfe einer Lewis-Säure, typischerweise Phosphorpentachlorid (PCl5), was zur Bildung von Isochinolin-Derivaten führt. Isochinoline sind aufgrund ihrer breiten biologischen Aktivität von großer Bedeutung, was diese Reaktion besonders wertvoll für die medizinische Chemie macht.
Eine herausragende Anwendung der Bischler-Napieralski-Reaktion ist ihre Rolle bei der Synthese von Neuroleptika wie Loxapin und Amoxapin. Diese Verbindungen gehören zur Klasse der Dibenzoxazepin-Derivate und werden als Antipsychotika eingesetzt. Loxapin wird zur Behandlung von Schizophrenie und bipolaren Störungen verwendet, während Amoxapin als Antidepressivum mit antipsychotischen Eigenschaften bekannt ist. Die zugrunde liegende Struktur dieser Verbindungen, ein Isochinolin-Ringsystem, ist entscheidend für ihre pharmakologische Aktivität, und ihre Synthese beruht häufig auf Varianten der Bischler-Napieralski-Reaktion.
Loxapin und Amoxapin verdeutlichen, wie eine grundlegende chemische Reaktion zur Herstellung von Medikamenten verwendet werden kann, die schwere psychische Erkrankungen behandeln. Loxapin, das erstmals in den 1970er Jahren synthetisiert wurde, wirkt vor allem durch die Blockierung von Dopaminrezeptoren, wodurch Symptome von Psychosen gemildert werden. Amoxapin hingegen hat eine doppelte Funktion: Es wirkt als Antidepressivum, indem es die Wiederaufnahme von Noradrenalin und Serotonin hemmt, und zeigt gleichzeitig antipsychotische Effekte durch seine Interaktion mit Dopaminrezeptoren.
Dank der Bischler-Napieralski-Reaktion reicht Napieralskis Beitrag zur Chemie weit über das Labor hinaus und hinein in die medizinische Praxis, wo seine Arbeit eine Schlüsselrolle bei der Entwicklung von Behandlungen für psychische Störungen spielt. Obwohl sein Name vielleicht nicht so bekannt ist wie der einiger seiner Zeitgenossen, bleibt sein Vermächtnis sowohl in der organischen Chemie als auch in der pharmazeutischen Forschung von großer Bedeutung.
Für die nach Hans Theodor Bucherer und Hermann Bergs benannte Synthese beziehungsweise die durch sie entstehenden Hydantoine gibt es im Labor und in der Technik zahlreiche praktische Anwendungen.
Bucherer absolvierte sein Abitur in Köln und studierte an den Universitäten München, Karlsruhe und Leipzig Chemie. Seine Dissertation schloss er 1893 unter Johannes Wislicenus in Leipzig ab. Der Titel seiner Arbeit lautete „Über einige Derivate des Keto-Hexens des Ketons der α Pimelinsäure“. Nach einiger Zeit bei der BASF wurde er 1901 Privatdozent an der Technischen Hochschule Dresden und folgte 1913 einem Ruf an die Technische Hochschule Berlin. Ab 1926 war er Professor für Chemische Technologie an der Technischen Hochschule München. In der Zeit von 1908 bis 1916 war er nebenbei in der chemischen Industrie tätig. Im Jahr 1935 wurde Bucherer emeritiert. 1944 erhielt er die Goethe-Medaille für Kunst und Wissenschaft.
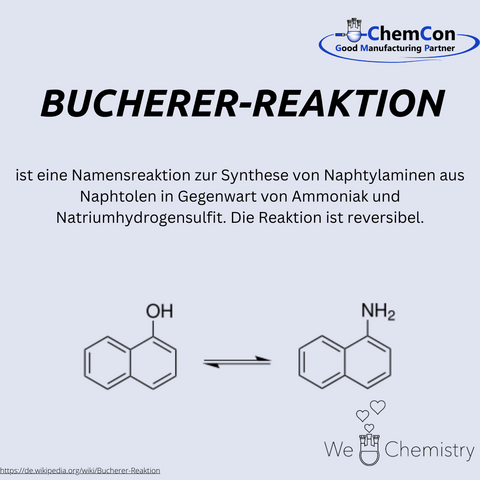
Neben der Bucherer-Bergs-Synthese entdeckte er auch die Bucherer-Reaktion, die es ermöglicht, Phenole und Naphthole etc. in die entsprechenden aromatischen Amine zu überführen.
Hydantoine werden in verschiedenen Anwendungen genutzt. Ausgehend von Hydantoin können heterocyclische Wirkstoffe wie zum Beispiel Phenytoin zur Dauerbehandlung von Epilepsie und Herzrhythmusstörungen hergestellt werden. Hydantoine können auch zur Herstellung von Zuckerderivaten verwendet werden. Außerdem sind sie ein Edukt zur Herstellung von Aminosäuren wie Methionin, von dem jährlich mehrere 100.000 Tonnen produziert werden.
Hydantoine sind ein Derivat des Imidazols. Ein weiteres Derivat davon ist Histamin, das durch Decarboxylierung der Aminosäure Histidin gewonnen werden kann. Eine Anwendung für Histamin ist als Histamin dihydrochlorid in Ceplene, zur Behandlung einer seltenen Art der Leukämie oder als positive Kontrolle in Allergietests.
Hans Theodor Bucherer, ein Name, der vielen vielleicht nicht geläufig ist, stellt einen Eckpfeiler in der Architektur der organischen Chemie dar. Geboren 1869, schnitzte sich dieser deutsche Chemiker durch seine akademischen Bestrebungen und bahnbrechende Forschung eine bedeutende Nische. Seine Reise, die an Universitäten wie München, Karlsruhe und Leipzig begann, mündete in einem Doktortitel unter dem geschätzten Johannes Wislicenus. Dieses solide Fundament katapultierte ihn in eine Welt akademischer Exzellenz.
Bucherers akademische Laufbahn ist gekennzeichnet durch seinen Aufstieg zu Professuren in Dresden, Berlin und München. Diese Rollen waren keine bloßen Titel; sie waren Plattformen, von denen aus er Wissen verbreitete und Neugier entfachte. Seine Beiträge zum Fachgebiet reichen jedoch weit über die Pädagogik hinaus. Die chemische Landschaft trägt die Prägung seines Einfallsreichtums, insbesondere in Form der Bucherer-Reaktion. Diese Umwandlung von Naphtholen in Naphthylamine und umgekehrt steht als Beweis seiner experimentellen Fähigkeiten.
Interessanterweise hat sich die Bucherer-Reaktion als eine praktikable Alternative zur Mitsunobu-Reaktion herausgestellt. Letztere ist zwar effektiv, beinhaltet jedoch oft giftige Reagenzien und Nebenprodukte. Im Gegensatz dazu präsentiert die Bucherer-Reaktion einen grüneren, umweltfreundlicheren Ansatz. Dieses Wiederaufleben des Interesses an einer älteren Reaktion unterstreicht die dauerhafte Relevanz grundlegender Forschung und das Potenzial, wertvolle Werkzeuge im Arsenal des Chemikers wiederzuentdecken.
Das Vermächtnis von Hans Theodor Bucherer ist ein Zeugnis für die Kraft intellektueller Neugier und Ausdauer. Sein Lebenswerk, charakterisiert durch die Bucherer-Reaktion und seine akademische Führung, inspiriert und beeinflusst weiterhin Chemiker weltweit. Während wir die Komplexitäten der modernen Chemie durchqueren, ist es wichtig, die Pioniere anzuerkennen, die den Grundstein gelegt haben, und Bucherer nimmt zweifellos einen prominenten Platz in diesem Pantheon wissenschaftlicher Helden ein.
John F. Hartwig ist ein renommierter amerikanischer Chemiker, der für seine Pionierarbeiten auf dem Gebiet der metallkatalysierten Reaktionen bekannt ist. Er wurde in den Vereinigten Staaten geboren und entwickelte bereits früh ein Interesse an der Chemie. Dieses Interesse führte ihn zu einer beeindruckenden akademischen Laufbahn: Er absolvierte seinen Bachelor-Abschluss in Chemie an der Princeton University und promovierte an der University of California, Berkeley. Anschließend forschte er als Postdoktorand am Massachusetts Institute of Technology (MIT), bevor er eine Professur an der Yale University übernahm. Später wechselte er an die University of Illinois und ist derzeit Professor an der University of California, Berkeley.
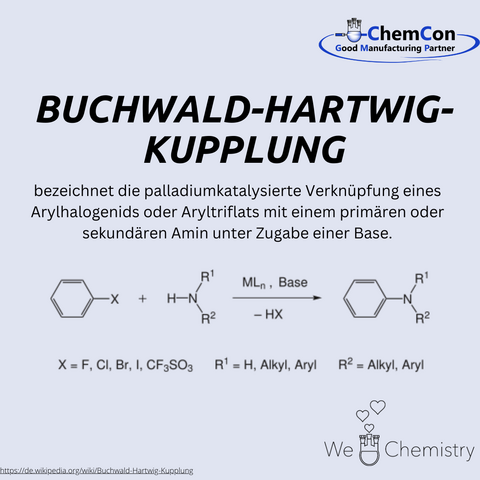
Seine Forschungsschwerpunkte liegen in der Entwicklung neuer katalytischer Prozesse, insbesondere im Bereich der Übergangsmetallkatalyse. Eine seiner bedeutendsten Errungenschaften ist die gemeinsam mit Stephen Buchwald entwickelte Buchwald-Hartwig-Amination. Diese Reaktion beschreibt die palladiumkatalysierte Kupplung von Arylhalogeniden oder Aryltriflaten mit primären oder sekundären Aminen in Anwesenheit einer Base. Diese Methode hat sich als äußerst effizient für die Synthese von Arylaminen erwiesen, die eine zentrale Rolle in der organischen Chemie spielen.
Die Buchwald-Hartwig-Amination hat die organische Chemie und insbesondere die pharmazeutische Industrie nachhaltig geprägt. Vor ihrer Entwicklung war die Herstellung von Arylaminen oft ineffizient, aufwendig und kostspielig. Durch die Einführung dieser palladiumkatalysierten Methode wurde es möglich, eine Vielzahl komplexer Amine unter milden Reaktionsbedingungen und mit hohen Ausbeuten herzustellen. Diese Fortschritte erleichterten die Synthese vieler pharmazeutisch relevanter Moleküle, da Arylamine in zahlreichen Wirkstoffen vorkommen. Heute ist die Buchwald-Hartwig-Amination ein unverzichtbares Werkzeug in der Arzneimittelforschung und -produktion und wird weltweit in akademischen und industriellen Laboren eingesetzt.
Auch ChemCon nutzt die Buchwald-Hartwig-Amination als integralen Bestandteil zur Herstellung pharmazeutischer Wirkstoffe und Zwischenprodukte. Die Flexibilität und Effizienz dieser Reaktion ermöglicht es ChemCon, komplexe Moleküle in hoher Reinheit und unter Einhaltung der strengen GMP-Richtlinien (Good Manufacturing Practice) zu produzieren. Dies ist essenziell, um den hohen Qualitätsanforderungen der pharmazeutischen Industrie gerecht zu werden. Durch die Anwendung dieser modernen Kupplungstechnologie kann ChemCon maßgeschneiderte Lösungen anbieten und innovative Wirkstoffe effizient entwickeln.
Für seine herausragenden Beiträge zur Chemie erhielt John F. Hartwig zahlreiche Auszeichnungen, darunter den American Chemical Society Award in Organometallic Chemistry und den Wolf Prize in Chemistry. Sein Einfluss auf die wissenschaftliche Gemeinschaft und die chemische Industrie ist immens. Seine Arbeiten bilden eine wichtige Grundlage für zukünftige Entwicklungen in der metallkatalysierten Chemie. Hartwigs Forschung hat nicht nur das Verständnis grundlegender chemischer Prozesse erweitert, sondern auch neue Anwendungen ermöglicht, die einen nachhaltigen Einfluss auf die moderne Arzneimittelentwicklung haben.
Ludwig Rainer Claisen geboren am 14. Januar 1851 in Köln war ein deutscher Chemiker. Er machte 1869 sein Abitur auf einem Gymnasium in Köln. Danach studierte er bis 1871 Chemie an der Universität Bonn und bis 1873 in Göttingen. Bis 1875 promovierte er in Bonn unter Kekulé mit der Arbeit „Beiträge zur Kenntniss des Mesityloxyds und des Phorons“ und wurde zunächst Kekulés Assistent.
Drei Jahre später habilitierte er und wurde anschließend als Privatdozent übernommen. Nach einigen Jahren am Owens College in Manchester und München folgte er dem Ruf an die RWTH Aachen, wo er zum Ordinarius für Chemie ernannt wurde. 1897 wechselte er an die Universität Kiel, wurde jedoch schon 1902 aus gesundheitlichen Gründen emeritiert. Zwei Jahre später forschte er in Berlin weiter bevor er ein privates Labor im Rheinland eröffnete.
Er war Mitglied der Bayrischen Akademie der Wissenschaften sowie Ehrenmitglied des Vereins deutscher Chemiker und wurde 1881 zum Mitglied der Leopoldina gewählt. Im gleichen Jahr entdeckte er die Claisen Kondensation. Außerdem sind einige Laborgeräte nach ihm benannt die „Claisenbrücke“ und der „Claisenkolben“.
Ludwig Claisen war ein deutscher Chemiker, geboren am 14. Januar 1851 in Köln. Bekannt ist er vor allem für die Entwicklung der nach ihm benannten Claisen-Umlagerung, eine grundlegende organische Reaktion. Claisen studierte Chemie an der Universität Bonn und später an der Universität Göttingen, wo er unter der Leitung von Friedrich Wöhler, einem der Pioniere der organischen Chemie, promovierte.
Während seiner akademischen Laufbahn leistete Claisen bedeutende Beiträge zur organischen Chemie, einschließlich seiner Arbeiten über Esterkondensationsreaktionen, die heute als Claisen-Kondensationen bekannt sind. Diese sind entscheidend für die Bildung von Kohlenstoff-Kohlenstoff-Bindungen in verschiedenen synthetischen Verfahren. Seine Forschung erweiterte wesentlich das Instrumentarium der synthetischen organischen Chemie und beeinflusste die Entwicklung von Pharmazeutika, Agrochemikalien und neuen Materialien.
Claisen hatte Positionen an mehreren renommierten Institutionen inne, darunter die Universität Berlin und die Universität Kiel. Seine Arbeit legte grundlegende Prinzipien fest, die für die Weiterentwicklung synthetischer Methodologien in der modernen Chemie entscheidend waren. Die von ihm entdeckten Reaktionen und die von ihm entwickelten Techniken sind nach wie vor integraler Bestandteil bei der Synthese komplexer molekularer Architekturen in akademischen und industriellen Umgebungen weltweit. Sein Vermächtnis zeichnet sich nicht nur durch die nach ihm benannten Reaktionen aus, sondern auch durch seine Rolle bei der Ausbildung der nächsten Generation von Chemikern während seiner Zeit als Professor.
Arthur C. Cope
...war ein US-amerikanischer Chemiker und Professor für organische Chemie am Massachusetts Institute of Technology (MIT) in Cambridge.
Er promovierte mit dem Thema “The synthesis of local anesthetics containing various phenylalkyl groups: Vinylethyl malonic ester and the cleavage of certain substituted malonic esters with sodium ethoxide” n der University of Wisconsin-Madison im Jahr 1932.
Während des Zweiten Weltkriegs führte er eine Reihe von Forschungen für chemische Waffen, Malariamittel und die Behandlung von Senfgasopfern durch.
Am MIT leitete er ab 1945 die Chemieabteilung. Die präparative organische Chemie war eines seiner Arbeitsgebiete, insbesondere Eliminierungs- und Kondensationsreaktionen. Daher wurden die Cope-Umlagerung, die Diaza-Cope-Umlagerung und die Cope-Eliminierung nach ihm benannt.
Elias James Corey ist ein US-amerikanischer Chemiker, der 1990 den Nobelpreis für Chemie für seine Entwicklung der Theorie und Methodik der organischen Synthese erhielt, insbesondere für seine Etablierung der Retrosynthese.
Corey wurde 1928 in Methuen, Massachusetts, als Sohn libanesischer Christen geboren. Er studierte Chemie am Massachusetts Institute of Technology, wo er 1948 seinen Bachelor-Abschluss und 1951 seinen Doktorgrad erwarb. Von 1951 bis 1959 war er Professor an der University of Illinois, wo er mit 27 Jahren zum ordentlichen Professor ernannt wurde. Seit 1959 ist er Professor an der Harvard University.
Corey hat über fünf Jahrzehnte lang in fast allen Bereichen der organischen Chemie geforscht und wichtige Beiträge zur Biochemie und zur modernen medizinischen Wissenschaft geleistet. Er hat zahlreiche Synthesemethoden und Reagenzien entwickelt, wie zum Beispiel das Pyridiniumchlorochromat oder die 1,3-Dithiane als Schutzgruppe für Carbonylverbindungen. Er hat auch die metallorganische Chemie, die katalytische asymmetrische Reaktion und den mechanistischen Einblick in die Bindungsbildung erforscht. Er war der erste, der Computer für die Gestaltung von Synthesewegen einsetzte.
Eines seiner bekanntesten Werke ist die Retrosynthese, eine logische Methode zur Planung der Synthese komplexer organischer Moleküle aus einfachen Vorläufern. Die Retrosynthese basiert auf dem Prinzip, dass eine komplexe Struktur in einfachere Teile zerlegt werden kann, indem man sich vorstellt, wie sie durch bekannte Reaktionen gebildet werden könnte. Diese Teile können dann weiter zerlegt werden, bis man zu verfügbaren Ausgangsmaterialien gelangt. Die Retrosynthese ist ein mächtiges Werkzeug für die Synthese von Naturstoffen, Arzneimitteln und anderen biologisch aktiven Verbindungen.
Corey hat mehrere hundert Totalsynthesen von Naturstoffen durchgeführt, darunter mehrere Prostaglandine, Steroide, Antibiotika und Alkaloide. Er hat auch das antivirale Medikament Oseltamivir (Tamiflu) synthetisiert, das gegen Influenza wirksam ist.
Corey ist einer der produktivsten und einflussreichsten Chemiker aller Zeiten. Er hat über 1000 wissenschaftliche Publikationen veröffentlicht und über 70 wissenschaftliche Preise erhalten. Er hat auch zahlreiche Industriechemiker sowie spätere Professoren und Nobelpreisträger wie Ryoji Noyori und Bengt Ingemar Samuelsson ausgebildet.
Elias James Corey wurde am 12. Juli 1928 in Methuen, Massachusetts, geboren und entwickelte sich zu einem der einflussreichsten Chemiker des 20. Jahrhunderts. Schon früh zeigte er ein großes Interesse an Wissenschaft und Mathematik, was ihn dazu brachte, am Massachusetts Institute of Technology (MIT) zu studieren. Dort promovierte er bereits im Alter von 22 Jahren und begann eine akademische Laufbahn, die ihn 1959 an die Harvard University führte. Dort blieb er über Jahrzehnte und prägte die organische Chemie nachhaltig. Sein bedeutendster Beitrag zur Wissenschaft war die Entwicklung der retrosynthetischen Analyse, einer Methode, die es ermöglicht, komplexe Moleküle durch Zerlegung in einfachere Bausteine zu planen. Diese bahnbrechende Technik revolutionierte die organische Synthese und wurde zur Standardstrategie in der modernen Chemie. Sein analytischer Ansatz half Chemikern weltweit, effiziente und präzise Syntheserouten für eine Vielzahl von Molekülen zu entwickeln. Für seine Arbeiten erhielt Corey zahlreiche Auszeichnungen, darunter 1990 den Nobelpreis für Chemie. Neben dem Nobelpreis wurde er auch mit weiteren Ehrungen wie der National Medal of Science und der Priestley Medal ausgezeichnet.
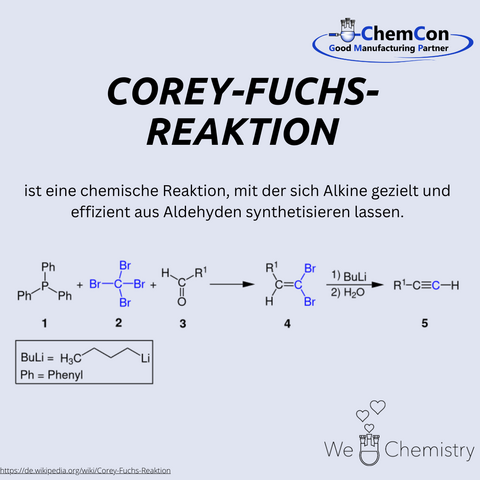
Ein spezifischer Beitrag von Corey zur synthetischen Chemie ist die Corey-Fuchs-Reaktion, eine Methode zur Synthese von Alkinen aus Aldehyden. Dabei werden Aldehyde mit Triphenylphosphin und Carbon Tetrabromid zu Dibromiden umgewandelt, die anschließend mit starken Basen zu Alkinen reagieren. Diese Reaktion ist besonders nützlich, um Terminalalkine effizient und gezielt herzustellen. Sie findet breite Anwendung in der pharmazeutischen Chemie und in der Herstellung komplexer organischer Verbindungen. ChemCon nutzt solche bewährten Methoden in der kundenspezifischen Synthese, um maßgeschneiderte Lösungen für pharmazeutische Anwendungen zu entwickeln. Durch die Integration solcher Reaktionen in die Prozessentwicklung kann ChemCon hochreine und spezifikationsgerechte Verbindungen für Forschungs- und Industriepartner bereitstellen. Die Fähigkeit, komplexe Synthesewege effizient umzusetzen, macht ChemCon zu einem wertvollen Partner für Unternehmen, die hochspezialisierte chemische Verbindungen benötigen.
Elias James Corey: Ein Chemiker, der die Welt veränderte
Elias James Corey wurde am 12. Juli 1928 in Methuen, Massachusetts, geboren. Er ist ein US-amerikanischer Chemiker und Nobelpreisträger. Corey ist emeritierter Professor an der Harvard University. Seine Studien über fünf Jahrzehnte umfassen nahezu alle Bereiche der Organischen Chemie und hatten entscheidende Auswirkungen auf die Biochemie und die moderne medizinische Wissenschaft.
Akademische Laufbahn
Corey erhielt seinen Bachelor-Abschluss in Chemie an der Harvard University im Jahr 1950. Anschließend promovierte er an der University of Illinois at Urbana-Champaign bei John C. Sheehan. Nach seiner Promotion arbeitete Corey als Postdoktorand am Massachusetts Institute of Technology (MIT) bei Robert Burns Woodward.
Im Jahr 1954 kehrte Corey an die Harvard University zurück, wo er eine Professur für Organische Chemie erhielt. Er blieb bis zu seiner Emeritierung im Jahr 2000 an der Harvard University.
Wissenschaftliche Errungenschaften
Corey hat im Laufe seiner Karriere zahlreiche bedeutende Beiträge zur Organischen Chemie geleistet. Zu seinen wichtigsten Errungenschaften gehören:
- Die Entwicklung neuer Synthesemethoden für komplexe Naturstoffe, darunter Steroide, Terpene und Alkaloide.
- Die Erforschung der Mechanismen organischer Reaktionen.
- Die Entwicklung neuer molekularer Katalysatoren.
Coreys Arbeiten haben dazu beigetragen, das Verständnis organischer Reaktionen zu vertiefen und neue Wege für die Synthese komplexer Moleküle zu eröffnen. Sie haben auch wichtige Auswirkungen auf die Biochemie und die moderne medizinische Wissenschaft gehabt.
Corey-Ghanem-Oxidation
Die Corey-Ghanem-Oxidation ist eine wichtige Synthesemethode für die Oxidation von Alkoholen zu Ketonen oder Aldehyden. Die Reaktion wurde 1967 von Elias James Corey und seinem Studenten Samir A. Ghanem entwickelt.
Die Corey-Ghanem-Oxidation verläuft in zwei Schritten. Im ersten Schritt wird der Alkohol mit einem starken Oxidationsmittel, wie z. B. Chromtrioxid, oxidiert. Im zweiten Schritt wird das entstehende Keton oder Aldehyd mit einem reduzierenden Agenten, wie z. B. Ammoniak, reduziert.
Die Corey-Ghanem-Oxidation ist eine vielseitige und effiziente Synthesemethode, die für eine Vielzahl von Alkoholen angewendet werden kann. Sie ist besonders nützlich für die Oxidation von empfindlichen Alkoholen, die mit anderen Oxidationsmethoden nicht stabil sind.
Auszeichnungen
Corey hat im Laufe seiner Karriere zahlreiche Auszeichnungen für seine wissenschaftlichen Leistungen erhalten. Zu seinen wichtigsten Auszeichnungen gehören:
- Der Nobelpreis für Chemie im Jahr 1990
- Die National Medal of Science im Jahr 1985
- Die Copley-Medaille der Royal Society im Jahr 1998
Corey ist einer der bedeutendsten Chemiker des 20. Jahrhunderts. Seine Arbeiten haben die Organische Chemie revolutioniert und haben wichtige Auswirkungen auf die Biochemie und die moderne medizinische Wissenschaft gehabt.
Theodor Curtius, ein angesehener deutscher Chemiker, dessen Name mit einigen Schlüsselentwicklungen in der Chemie verbunden ist, wurde in Duisburg im industriellen Ruhrgebiet Deutschlands geboren. Seine Reise in die Welt der Chemie begann an einigen der besten deutschen Universitäten, unter der Anleitung von Robert Bunsen an der Universität Heidelberg und Hermann Kolbe an der Universität Leipzig, wo er 1882 promovierte.
Sein beruflicher Weg war geprägt von bedeutenden Positionen und Beiträgen. Von 1884 bis 1886 arbeitete er unter Adolf von Baeyer an der Universität München, eine Erfahrung, die seine Forschungsfähigkeiten schärfte und ihn auf zukünftige akademische Führungsrollen vorbereitete. Anschließend leitete er bis 1889 das Institut für analytische Chemie an der Universität Erlangen und bewies seine Kompetenz und Hingabe für das Fach.
Curtius’ Karriere setzte sich fort, als er den Lehrstuhl für Chemie an der Universität Kiel übernahm. Während seiner Amtszeit wurde er für seine Produktivität und Forschungskompetenz anerkannt, was ihm 1895 die Ernennung zum Geheimen Regierungsrat einbrachte. Seine Leistungen führten ihn 1897 zur Universität Bonn, wo er die renommierte Position einnahm, die zuvor August Kekulé innehatte. Im folgenden Jahr kehrte er zu seiner Alma Mater, der Universität Heidelberg, zurück, wo er Victor Meyer als Professor für Chemie nachfolgte. Bis zu seiner Pensionierung im Jahr 1926 blieb er eine zentrale Figur und prägte die Köpfe und Karrieren zukünftiger Chemiker.
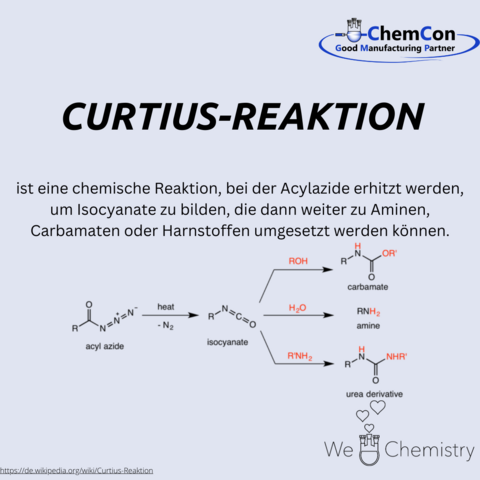
Einer seiner bedeutendsten wissenschaftlichen Beiträge ist die Curtius-Umlagerung, eine wichtige Reaktion in der organischen Chemie, die die thermische Zersetzung von Acylaziden in Isocyanate beinhaltet. Diese sind Schlüsselintermediate bei der Synthese von Aminen, Carbamaten und Harnstoffen und haben breite Anwendungen in der Pharmazie und Polymerwissenschaft, was Curtius' nachhaltigen Einfluss auf die chemische Synthese zeigt.
Außerhalb des Labors war Curtius ebenso leidenschaftlich an Musik und der Natur interessiert. Er war ein begeisterter Bergsteiger und Gründer der Kieler Sektion des Verbandes der Deutschen und Österreichischen Alpenvereine im Jahr 1894, eine Gruppe, die er großzügig unterstützte. Seine musikalischen Talente zeigte er durch seine Kompositionen und Auftritte bei Konzerten und ergänzte seine Persönlichkeit über seine wissenschaftlichen Errungenschaften hinaus. Während seiner Zeit in München entwickelte er eine enge Freundschaft mit Christian Klucker, einem renommierten Alpinistenführer, mit dem er zahlreiche Bergtouren unternahm.
Das Leben und Werk von Theodor Curtius war geprägt von strenger wissenschaftlicher Forschung und einer tiefen Wertschätzung für Kunst und Natur. Er verstarb am 8. Februar 1928 in Heidelberg und hinterließ ein Erbe, das die Bereiche Chemie und darüber hinaus weiterhin beeinflusst. Seine Beiträge werden nicht nur durch seine wissenschaftlichen Entdeckungen, sondern auch durch seine persönlichen Leidenschaften in Erinnerung gehalten, die ihn zu einem vielseitigen Gelehrten und Menschen machten. Sein Leben ist ein Zeugnis dafür, welchen Einfluss man haben kann, wenn man die Lücke zwischen Wissenschaft und Geisteswissenschaften überbrückt.
Otto Paul Hermann Diels und Kurt Alder:
Diels wurde in Hamburg geboren und zog mit seiner Familie nach Berlin, wo er Chemie studierte. Er blieb bis 1915 an der Universität Berlin und nahm dann eine Stelle an der Universität Kiel an, wo er bis zu seiner Pensionierung im Jahr 1945 blieb. Während seiner Zeit in Kiel arbeitete er mit Kurt Alder an der Entwicklung der Diels-Alder-Reaktion.
Alder wurde im Industriegebiet von Königshütte in Schlesien geboren. Als Königshütte ein Hafen von Polen wurde, zog er nach Berlin. Er promovierte in Kiel, wo er Herrn Diels kennenlernte. Alder erhielt mehrere Ehrentitel und andere Auszeichnungen, darunter 1950 den Nobelpreis für Chemie, den er sich mit seinem Lehrer Diels für ihre Arbeiten über die Diels-Alder-Reaktion teilte.
Otto Dimroth, geboren am 28. März 1872 in Bayreuth, Deutschland, ist als bedeutende Persönlichkeit der organischen Chemie bekannt. Seine Beiträge zum Fachgebiet sind vielfältig und wirkungsvoll, wobei die Dimroth-Umlagerung und der Dimroth-Kühler zu seinen bemerkenswertesten Innovationen zählen.
Dimroth absolvierte seine Ausbildung an der Universität München und der Universität Erlangen, wo er von renommierten Chemikern betreut wurde. Diese frühe Auseinandersetzung mit fortgeschrittener chemischer Synthese und Reaktionsmechanismen weckte seine Leidenschaft und legte eine solide Grundlage für seine zukünftigen Forschungen. Seine akademische Laufbahn führte ihn zu Professuren an mehreren deutschen Universitäten, darunter die Universität Jena und die Universität Würzburg. Während seiner gesamten Karriere zeichnete sich Dimroth durch einen akribischen Ansatz in der chemischen Synthese und ein tiefes Verständnis der Reaktionsmechanismen aus.
Unter seinen zahlreichen Beiträgen sticht die Entwicklung der Dimroth-Umlagerung hervor. Diese Reaktion beinhaltet die Wanderung von Substituenten innerhalb eines Moleküls, insbesondere innerhalb von 1,2,3-Triazolen, und findet breite Anwendung in der Synthese komplexer organischer Verbindungen. Die Umlagerung kann als die Umwandlung eines substituierten 1,2,3-Triazols in ein anderes substituiertes 1,2,3-Triazol zusammengefasst werden, die durch starke Basen oder Hitze erleichtert wird. Diese Reaktion ist besonders wertvoll in der Heterocyclenchemie und spielt eine entscheidende Rolle bei der Herstellung verschiedener stickstoffhaltiger Verbindungen, die in der Pharma- und Agrarchemie verwendet werden.
Eine weitere bedeutende Erfindung von Dimroth ist der Dimroth-Kühler, auch bekannt als Dimroth-Kondensator. Dieses Gerät wird in Destillationsprozessen verwendet und ist besonders effektiv für Rückflussanwendungen. Sein einzigartiges Design, das eine gewundene Innentube umfasst, durch die Kühlwasser fließt und von den zu kondensierenden Dämpfen umgeben ist, bietet eine größere Oberfläche für den Wärmeaustausch. Dies macht den Dimroth-Kühler hoch effizient und zuverlässig, und er hat sich in chemischen Laboren weltweit, insbesondere in der organischen Synthese, bei der präzise Temperaturkontrolle entscheidend ist, bewährt.
Die Beiträge von Otto Dimroth zur Chemie gehen weit über seine namensgebenden Reaktionen und Geräte hinaus. Seine Arbeit hat Generationen von Chemikern beeinflusst und Fortschritte sowohl in der akademischen Forschung als auch in industriellen Anwendungen ermöglicht. Die Prinzipien der Dimroth-Umlagerung werden weiterhin erforscht und in der modernen chemischen Synthese angewendet, was die anhaltende Relevanz seiner Entdeckungen zeigt.
Dimroth verstarb am 16. Mai 1940, doch sein Erbe lebt durch die vielen Chemiker weiter, die auf seinen grundlegenden Arbeiten aufbauen. Sein Leben und seine Karriere dienen als Inspiration und unterstreichen die Bedeutung von Neugier, Hingabe und Innovation in wissenschaftlichen Bestrebungen. Von seinen frühen Tagen als Student in Deutschland bis zu seinen einflussreichen Rollen als Professor und Forscher hat Otto Dimroth durch seine tiefgreifende wissenschaftliche Neugier und seine bedeutenden Errungenschaften einen unauslöschlichen Eindruck in der Chemie hinterlassen. Seine Entwicklung der Dimroth-Umlagerung und des Dimroth-Kühlers sind Zeugnisse seiner Genialität und haben seinen Platz in den Annalen der Wissenschaftsgeschichte gesichert. Während die Komplexitäten chemischer Reaktionen und Prozesse weiter erforscht werden, bleibt Otto Dimroths Arbeit ein Leitstern, der uns an die Kraft menschlicher Genialität bei der Entschlüsselung der Geheimnisse der natürlichen Welt erinnert.
Karl Heinz Dötz war eine bemerkenswerte Persönlichkeit auf dem Gebiet der organischen Chemie, der durch seine bahnbrechenden Beiträge einen bleibenden Einfluss auf die moderne chemische Synthese hinterlassen hat. Geboren 1943 in Deutschland, begann Dötz eine wissenschaftliche Laufbahn, die ihn zu einem der angesehensten Chemiker seiner Zeit machen sollte.
Dötz' akademische Karriere nahm ihren Anfang mit seinem Chemiestudium, in dem er früh eine ausgeprägte Begabung für komplexe Problemlösungen und Innovationen zeigte. Er promovierte unter der Anleitung einiger führender Chemiker jener Zeit und entwickelte dabei ein fundiertes Wissen in der organischen Chemie. Seine Arbeiten während dieser Zeit legten den Grundstein für einen bahnbrechenden Beitrag zum Fachgebiet: die Dötz-Reaktion.
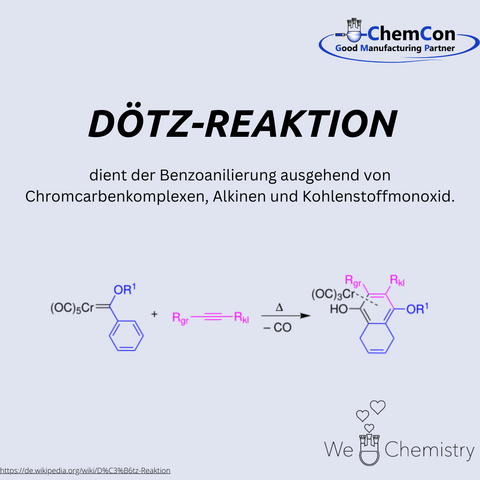
Die Dötz-Reaktion, auch bekannt als Benzanellierungsreaktion, ist eine Methode zur Synthese aromatischer Verbindungen aus Chromcarbenkomplexen, Alkinen und Kohlenmonoxid. Diese Reaktion wurde erstmals von Dötz in den späten 1970er Jahren beschrieben und erregte schnell Aufmerksamkeit aufgrund ihrer Eleganz und Nützlichkeit. Der Prozess umfasst die Bildung eines hochreaktiven Chromcarben-Intermediats, das anschließend mit einem Alkin und Kohlenmonoxid reagiert, um ein substituiertes Phenol oder einen aromatischen Ring zu erzeugen. Die Reaktion ist hoch regioselektiv und bietet einen direkten Weg zu komplexen aromatischen Strukturen, die oft schwer auf anderem Wege zu gewinnen sind.
Ein Grund für die anhaltende Bedeutung der Dötz-Reaktion ist ihre Vielseitigkeit. Sie stellt Chemikern ein mächtiges Werkzeug zur Verfügung, um Benzolringe zu konstruieren, die grundlegende Bausteine in der organischen Chemie darstellen. Aromatische Verbindungen sind allgegenwärtig in der Natur und finden sich in einer Vielzahl von Naturstoffen, Pharmazeutika und Materialien. Die Fähigkeit, diese Strukturen effizient zu synthetisieren, macht die Dötz-Reaktion in verschiedenen Forschungs- und Industriebereichen unverzichtbar.
Heute wird die Dötz-Reaktion weiterhin häufig genutzt, insbesondere bei der Synthese von Naturstoffen und komplexen organischen Molekülen. Ihre Anwendung erstreckt sich bis in die pharmazeutische Industrie, wo sie bei der Herstellung von Wirkstoffkandidaten und anderen biologisch aktiven Verbindungen eingesetzt wird. Die Effizienz und Selektivität der Reaktion machen sie zu einer attraktiven Wahl für Chemiker, die komplizierte molekulare Architekturen präzise erschaffen wollen.
Das Vermächtnis von Karl Heinz Dötz geht jedoch über seine gleichnamige Reaktion hinaus. Im Laufe seiner Karriere leistete er zahlreiche Beiträge auf dem Gebiet der metallorganischen Chemie und betreute eine Generation von Chemikern, die ihrerseits bedeutende Beiträge geleistet haben. Sein Werk steht beispielhaft für die Kraft innovativen Denkens in der Wissenschaft, wo eine einzige Reaktion neue Forschungs- und Anwendungsfelder eröffnen kann.
Zusammenfassend lässt sich sagen, dass das Leben und Wirken von Karl Heinz Dötz einen tiefgreifenden Einfluss auf die Chemie hatte. Die Dötz-Reaktion bleibt ein Grundpfeiler der modernen Synthesechemie, und ihre heutige Anwendung zeugt von der Genialität und Weitsicht ihres Schöpfers. Auch in der Zukunft werden die Prinzipien, die der Dötz-Reaktion zugrunde liegen, zweifellos weitere Entdeckungen und Fortschritte in den chemischen Wissenschaften inspirieren.
Emil Erlenmeyer Jr. trat aus dem Schatten einer bemerkenswerten Abstammung hervor und führte das Erbe seines Vaters, Emil Erlenmeyer Sr., einer Leuchte in der Welt der Chemie, weiter. Geboren in einer Umgebung, die reich an wissenschaftlichem Diskurs und Innovation war, neigte Erlenmeyer Jr. natürlich zu den Wissenschaften, insbesondere zur Chemie, der er sich mit Eifer und Hingabe widmete.
Erlenmeyer Jr. erhielt seine Ausbildung an einigen der besten Einrichtungen Europas und entwickelte ein tiefes Verständnis für chemische Prozesse. Sein akademischer Weg wurde stark von den Errungenschaften und Methoden seines Vaters beeinflusst. Emil Erlenmeyer Sr., bekannt für die Erfindung des Erlenmeyerkolbens im Jahr 1860, war eine zentrale Figur in der Chemie des 19. Jahrhunderts. Seine Beiträge gingen über dieses ikonische Laborgerät hinaus; er spielte eine entscheidende Rolle bei der Entwicklung der Strukturtheorie in der organischen Chemie, die besagt, dass die Anordnung der Atome in einem Molekül dessen Eigenschaften bestimmt.
Einer der bedeutenden Beiträge von Emil Jr. zum Fachgebiet war die "Erlenmeyer-Synthese", ein Prozess, der die Bildung von β-Hydroxyketonen aus α-Diazoketonen umfasst. Diese Reaktion unterstrich seine Fähigkeit, komplexe Techniken der organischen Chemie zu nutzen, um neue Syntheseprozesse zu erleichtern, die langfristige Auswirkungen auf die Herstellung verschiedener organischer Verbindungen, insbesondere in der Pharmazie, hatten.
Der Einfluss seines Vaters war in Erlenmeyers Karriere unverkennbar. Erlenmeyer Seniors Lehren boten nicht nur eine solide Grundlage in den Grundprinzipien der Chemie, sondern weckten auch eine Neugier und den Antrieb zur Innovation. Dieser väterliche Einfluss war deutlich erkennbar, als Emil Jr. die wissenschaftlichen Ideen seines Vaters erweiterte und half, den Übergang von traditionellen chemischen Praktiken zu moderneren Ansätzen zu bewältigen, die heute in wissenschaftlichen und medizinischen Forschungsumgebungen Standard sind.
Emil Erlenmeyer Seniors Rolle als Pionier spiegelt sich in seinen Beiträgen zur organischen Chemie wider, insbesondere durch seine Arbeit über die Struktur und das Verhalten verschiedener organischer Verbindungen. Seine Forschung ebnete den Weg für die Akzeptanz und Erweiterung der Strukturtheorie in der organischen Chemie, die grundlegend die Art und Weise verändert hat, wie Chemiker heute Moleküle verstehen und manipulieren.
Durch seine eigenen Innovationen und Beiträge ehrte Emil Erlenmeyer Jr. nicht nur das Erbe seines Vaters, sondern half auch, eine Verbindung zwischen vergangenen und zeitgenössischen chemischen Praktiken herzustellen. Seine Arbeit beeinflusst die moderne Chemie weiterhin, insbesondere durch Methoden und Synthesetechniken, die für die Entwicklung neuer Medikamente und Behandlungen unerlässlich geworden sind. Auf diese Weise haben sowohl Emil Erlenmeyer Sr. als auch Jr. einen dauerhaften Einfluss auf das Fachgebiet hinterlassen, indem sie zeigen, wie das Fackel der wissenschaftlichen Untersuchung erfolgreich von einer Generation zur nächsten weitergereicht werden kann, wobei jede auf dem Fundament der letzten aufbaut.
Albert Eschenmoser war einer der bedeutendsten Chemiker des 20. Jahrhunderts und hinterließ ein beeindruckendes wissenschaftliches Erbe. Geboren 1925 in der Schweiz, begann er seine akademische Laufbahn an der ETH Zürich, wo er später als Professor wirkte. Sein Forschungsschwerpunkt lag im Bereich der organischen Chemie, insbesondere in der Synthese und Strukturaufklärung komplexer Naturstoffe. Er leistete bahnbrechende Beiträge zur Totalsynthese von Vitamin B12, einem der anspruchsvollsten Projekte in der organischen Chemie, das er gemeinsam mit Robert Burns Woodward erfolgreich abschloss. Diese Leistung machte ihn weltweit bekannt und brachte ihm zahlreiche wissenschaftliche Auszeichnungen ein, darunter die Copley-Medaille der Royal Society und die Wolf-Preis in Chemie.
Neben der Vitamin-B12-Synthese widmete sich Eschenmoser der Frage nach den chemischen Grundlagen des Lebens. Seine Arbeiten zur Präbiotischen Chemie trugen wesentlich zum Verständnis der möglichen Entstehung von Nukleinsäuren bei. Er untersuchte alternative Nukleinsäurestrukturen und entwickelte das Konzept der Eschenmoser-Fragmentierung, eine Reaktion, die in der organischen Synthese große Bedeutung erlangte. Sein tiefes Verständnis für Naturstoffe und deren Biosynthese hatte weitreichenden Einfluss auf die pharmazeutische Forschung und die Entwicklung neuer Wirkstoffe.
Auch heute noch sind seine Erkenntnisse in der modernen Medizin von großer Bedeutung. Die synthetische Herstellung von Naturstoffen ermöglicht es, hochwirksame Arzneimittel gezielt zu entwickeln, die auf natürlichen Vorbildern basieren. Hier setzt ChemCon an: Als Spezialist für Auftragsherstellung und kundenspezifische Synthesen entwickelt ChemCon Naturstoffe synthetisch, um sie für Forschung und Industrie verfügbar zu machen. Gerade im Bereich der Pharmaindustrie sind maßgeschneiderte Naturstoffderivate essenziell für die Wirkstoffentwicklung. Die Expertise von ChemCon in der GMP-konformen Auftragsproduktion stellt sicher, dass Kunden hochreine und verlässliche Substanzen erhalten, die den höchsten regulatorischen Anforderungen entsprechen.
Die Forschung von Albert Eschenmoser lebt weiter in der modernen organischen Chemie und beeinflusst bis heute die Entwicklung neuer Medikamente. Seine Arbeiten zeigen, wie essenziell die Verbindung zwischen Grundlagenforschung und angewandter Wissenschaft ist – ein Ansatz, den auch ChemCon verfolgt, um innovative Lösungen für die pharmazeutische und biotechnologische Industrie bereitzustellen. Die Möglichkeit, Naturstoffe gezielt zu synthetisieren, eröffnet neue Wege in der Wirkstoffforschung und unterstreicht die Bedeutung der chemischen Synthese für die Medizin der Zukunft.
Alexei Jewgrafowitsch Faworski, ein bedeutender russischer Chemiker, wurde am 14. März 1860 geboren und verstarb am 8. August 1945. Faworski trug wesentlich zur Entwicklung der organischen Chemie bei, insbesondere durch die Entdeckung und Erforschung der nach ihm benannten Faworski-Umlagerung.
Faworski begann seine wissenschaftliche Karriere an der Universität Sankt Petersburg, wo er später Professor wurde. Seine Arbeit konzentrierte sich auf die Mechanismen organischer Reaktionen und die Synthese komplexer organischer Verbindungen. Die Faworski-Umlagerung, eine von ihm entdeckte Reaktion, ist eine bemerkenswerte Transformation, bei der enolisierbare α-Halogenketone durch Behandlung mit Hydroxiden zu Carbonsäuren umgelagert werden. Interessanterweise lassen sich durch den Einsatz anderer Basen auch Carbonsäureester und Carbonsäureamide darstellen. Die Reaktion verläuft über die Bildung eines Enolats, gefolgt von einer intramolekularen Umlagerung und Hydrolyse eines intermediären Cyclopropanons.
Ein bedeutendes Anwendungsgebiet der Faworski-Umlagerung ist die Synthese von Cubanen. Cubane, eine Verbindung mit der chemischen Formel C₈H₈, zeichnet sich durch ihre ungewöhnliche Struktur aus, bei der alle Kohlenstoff-Kohlenstoff-Bindungswinkel 90° betragen. Diese Struktur verleiht Cubanen besondere physikalische und chemische Eigenschaften. Die Synthese von Cubanen, die erstmals 1964 von Philip Eaton und Thomas Cole durchgeführt wurde, ist anspruchsvoll und umfasst mehrere Schritte. Einer der Schlüsselschritte in diesem komplexen Syntheseweg ist die Faworski-Umlagerung.
Cubane sind aufgrund ihrer einzigartigen Struktur und hohen Spannungsenergie von großem Interesse. Die rechtwinkligen Bindungswinkel, die in der Natur äußerst selten vorkommen, machen Cubane zu Verbindungen mit hoher Dichte und Stabilität. Diese Eigenschaften machen Cubane besonders nützlich in verschiedenen Anwendungen, darunter in der Medizin und Materialwissenschaft. Beispielsweise werden Cubane in der Entwicklung von energiereichen Treibstoffen und Explosivstoffen sowie in der Pharmakologie als stabile Gerüststrukturen für die Entwicklung neuer Medikamente verwendet.
Durch seine Forschung und Entdeckungen hat Alexei Jewgrafowitsch Faworski einen bleibenden Einfluss auf die organische Chemie ausgeübt. Seine Arbeiten zur Faworski-Umlagerung haben nicht nur zu grundlegenden Erkenntnissen über Reaktionsmechanismen geführt, sondern auch bedeutende Anwendungen in der Synthese komplexer Moleküle ermöglicht, darunter die bemerkenswerte Verbindung Cubane. Seine kreative und innovative Herangehensweise an chemische Probleme bleibt ein inspirierendes Erbe in der Welt der Chemie.
Hans Finkelstein ist eine bedeutende Figur in der Chemiegeschichte, insbesondere in der organischen Halogenchemie. Geboren im späten 19. Jahrhundert, widmete sich der deutsche Chemiker intensiv der Erforschung von Halogenaustauschreaktionen und hinterließ mit der nach ihm benannten Finkelstein-Reaktion ein Vermächtnis, das bis heute in der chemischen Industrie von Bedeutung ist.
Finkelstein studierte Chemie an einer renommierten deutschen Universität, wo er sich frühzeitig für organische Syntheseverfahren interessierte. Sein Hauptforschungsgebiet lag in der Substitution von Halogenatomen in organischen Verbindungen. Besonders bemerkenswert war seine Entdeckung, dass sich Chlor- oder Brom-Substituenten in organischen Molekülen unter Einsatz von Natriumiodid in Aceton effizient durch Iodid ersetzen lassen. Diese Erkenntnis führte zur Entwicklung der Finkelstein-Reaktion, die als elegante Methode für den Halogenaustausch in der organischen Synthese gilt.
Die Finkelstein-Reaktion ist eine nukleophile Substitutionsreaktion (SN2), bei der ein Halogenatom durch ein anderes ersetzt wird. Sie spielt eine entscheidende Rolle in der Herstellung von organischen Iodverbindungen, die wiederum als Schlüsselrohstoffe in der pharmazeutischen Synthese, der Agrochemie und der Materialwissenschaft genutzt werden. Die einfache Handhabung und hohe Selektivität dieser Reaktion machen sie zu einem Standardverfahren in der chemischen Forschung und Produktion.
Das Vermächtnis von Hans Finkelstein ist auch heute noch in der chemisch-pharmazeutischen Industrie spürbar. Viele moderne Synthesemethoden basieren auf seinen Prinzipien oder wurden durch seine Entdeckungen inspiriert. Besonders in der Produktion von Wirkstoffen und Spezialchemikalien sind Halogenaustauschreaktionen von großer Bedeutung.
Die ChemCon GmbH führt das Erbe der präzisen und hochwertigen Syntheseverfahren fort und unterstützt die chemisch-pharmazeutische Industrie mit maßgeschneiderten Lösungen. Als Spezialist für Auftragsentwicklung & Herstellung bietet ChemCon innovative Wege zur Produktion von hochreinen Wirkstoffen, Zwischenprodukten und Spezialchemikalien. Dank umfassender Expertise in der Syntheseentwicklung ermöglicht das Unternehmen individuelle Synthesewege für anspruchsvolle Projekte – von der Laborentwicklung bis zur GMP-Produktion.
Durch die Verbindung von klassischer organischer Chemie mit modernster Technologie bleibt ChemCon ein verlässlicher Partner für die Pharma- und Chemiebranche. Die Prinzipien, die einst Hans Finkelstein mit seiner Forschung legte, leben heute in den innovativen Entwicklungen und maßgeschneiderten Synthesestrategien von ChemCon weiter.
Emil Fischer, eine herausragende Persönlichkeit in der Chemie, wurde am 9. Oktober 1852 in Euskirchen, Deutschland, geboren. Seine frühen Jahre wurden von einer soliden Bildung geprägt, die er seinem Vater, einem erfolgreichen Geschäftsmann, verdankte. Dieser vermittelte ihm Werte wie Disziplin und Neugierde. Fischers akademischer Weg begann an der Universität Bonn, wo er zunächst Chemie studierte. Doch erst sein Wechsel zur Universität Straßburg markierte den eigentlichen Beginn seiner bemerkenswerten Karriere. Dort entflammte seine Leidenschaft für die organische Chemie unter der Anleitung von Adolf von Baeyer.
Seine Doktorarbeit, die er 1874 abschloss, konzentrierte sich auf Phenolphthalein und legte den Grundstein für seine zukünftigen Forschungen. Nach seiner Promotion arbeitete Fischer kurzzeitig an der Universität München, bevor er eine Stelle an der Universität Erlangen annahm. Dort begann Fischer, bedeutende Fortschritte in der Erforschung von Purinen und Zuckern zu machen. Seine präzisen Studien über die Struktur und Synthese dieser Verbindungen brachten ihm weitreichende Anerkennung ein und führten schließlich zu seiner Berufung an die Universität Würzburg im Jahr 1888 und später an die Universität Berlin im Jahr 1892.
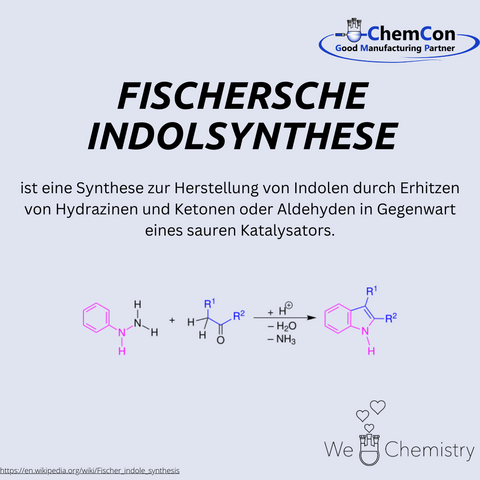
Eine seiner bemerkenswertesten Leistungen war seine Arbeit zur Stereochemie von Zuckern und Purinen. Seine bahnbrechenden Forschungen über die Struktur von Glukose und anderen Zuckern revolutionierten die Kohlenhydratchemie. Durch die Entwicklung der Fischer-Projektion, einer Methode zur Darstellung der dreidimensionalen Struktur von Molekülen auf einer zweidimensionalen Ebene, gab er Chemikern ein mächtiges Werkzeug an die Hand, um die räumliche Anordnung von Atomen in einem Molekül zu visualisieren und zu verstehen. Dieser Durchbruch ermöglichte nicht nur das Verständnis vieler Zuckerstrukturen, sondern ebnete auch den Weg für Fortschritte in der Biochemie und Molekularbiologie.
Neben seinen Beiträgen zur Kohlenhydratchemie waren Fischers Arbeiten über Purine ebenso bahnbrechend. Er identifizierte die Struktur von Harnsäure und Koffein, und seine Synthese verschiedener Purine legte den Grundstein für die Entwicklung von Pharmazeutika und das Verständnis der Nukleinsäuren, den Bausteinen von DNA und RNA. Seine Arbeiten auf diesem Gebiet waren so bedeutend, dass ihm 1902 der Nobelpreis für Chemie verliehen wurde.
Abgesehen von seinen wissenschaftlichen Leistungen war Fischer auch für sein Engagement in der Lehre und Betreuung bekannt. Er förderte zahlreiche Studenten, die später selbst zu bedeutenden Chemikern wurden. Fischers Fähigkeit, Talent zu inspirieren und zu fördern, war ein Beweis für seine Leidenschaft für die Chemie und sein Engagement für den Fortschritt des Fachgebiets.
Trotz persönlicher Herausforderungen, einschließlich des Verlusts seiner ersten Frau und gesundheitlicher Probleme, blieb Fischer bis zu seinem Tod am 15. Juli 1919 unerschütterlich in seinen wissenschaftlichen Bestrebungen. Sein Vermächtnis lebt nicht nur in den zahlreichen Auszeichnungen und Ehrungen weiter, die er erhielt, sondern auch in den nachhaltigen Auswirkungen seiner Arbeit auf die moderne Wissenschaft.
Emil Fischers Leben und Karriere verkörpern das unermüdliche Streben nach Wissen und den tiefgreifenden Einfluss, den eine einzelne Person auf die wissenschaftliche Gemeinschaft haben kann. Seine Beiträge wirken bis heute nach, beeinflussen die zeitgenössische Forschung und inspirieren zukünftige Generationen von Chemikern.
1850 studierte Friedel in Straßburg Naturwisschenschaften und setzte dies nach einer Unterbrechung 1852 an der Sorbonne fort. Von 1856 bis 1870 arbeitete er als Kurator der Mineraliensammlung der École des Mines. Während dieser Zeit vertiefte er seine chemischen Kenntnisse unter Charles Adolphe Wurtz im Labor der École de médecine. 1861 lernten sich hier Charles Friedel und James Mason Crafts kennen. James studierte nach dem Bachelor of Science (1858) 1859 an der Bergakademie Freiberg, 1860 an der Universität Heidelberg und 1861 an der École de Médecine in Paris. Im Jahr 1877 entdeckten sie die katalytische Wirkung von Aluminiumchlorid bei Reaktionen von Aromaten mit Alkylhalogeniden, heute bekannt als Friedel-Crafts-Reaktionen. Dies ist eine grundlegende Reaktion, die jeder Chemiker lernt und auch in den Laboren der ChemCon durchgeführt wird.
Tohru Fukuyama ist eine herausragende Persönlichkeit auf dem Gebiet der organischen Chemie, bekannt für seine bahnbrechenden Forschungen und die Entwicklung innovativer Synthesemethoden, insbesondere der Fukuyama-Amin-Synthese. Diese Methode revolutionierte die Synthese sekundärer Amine, indem sie einen neuartigen Weg über Nosylamide eröffnete und die Thiolat-induzierte Eliminierung nutzte, um diese Umwandlung zu erreichen. Abgesehen von ihren technischen Vorzügen hat die Fukuyama-Amin-Synthese den Horizont für die Synthese von Polyamiden erweitert und zur Verbesserung der Festphasensynthesetechniken beigetragen. Die Festphasensynthese kann auch zur Herstellung von Biopolymeren verwendet werden. Fukuyamas akademische Laufbahn ist von zahlreichen Errungenschaften geprägt, darunter wichtige Veröffentlichungen und die Betreuung der nächsten Generation von Chemikern. Seine Arbeit hat wesentlich zu Fortschritten in der Pharmazie und den Materialwissenschaften beigetragen, was seinen großen Einfluss sowohl auf die akademische Forschung als auch auf praktische Anwendungen in der chemischen Synthese zeigt.
Sigmund Gabriel wurde am 07.November 1851 in Berlin geboren. Er studierte und promovierte bis 1874 in Heidelberg bei Robert Wilhelm Bunsen. Bis 1921 war er Professor an der Berliner Universität wo er organische Stickstoff-Verbindungen untersuchte. 1887 entwickelte er die nach ihm benannte Gabriel Synthese zur Darstellung von primären Alkylaminen. Im Jahr 1888 wurde er außerdem zu einem Mitglied der Leopoldina gewählt.
Die Reaktion ist ein reines Laborverfahren aufgrund schlechter Atomökonomie. Die Synthese primärer Amine aus Halogenalkanen und Ammoniak ist nicht möglich da dabei Amine anderer Alkylierungstufen gebildet werden. Ein Beispiel für ein sekundäres Amin ist das Piperidin welches vom dänischen Chemiker Hans Christian Ørsted erstmals isoliert wurde.
Victor Grignard:
Nicht bestandene Aufnahmeprüfungen in Mathematik - Militärdienst - Nobelpreisträger für Chemie
Obwohl er die Aufnahmeprüfung zunächst nicht bestand, versuchte er es nach einem Jahr beim Militär erneut und war erfolgreich. Das reichte ihm aber nicht und er wechselte zur Chemie.
Dank Dr. Grignard, der 1912 (zusammen mit Paul Sabatier) den Nobelpreis für Chemie erhielt, ist es heute möglich, Synthesen mit fortschrittlichen Methoden in der organischen Chemie durchzuführen.
Grignard veröffentlichte rund 170 wissenschaftliche Artikel über seine Arbeit und arbeitete bis zu seinem Tod an einer großen chemischen Enzyklopädie in französischer Sprache.
Auch wenn er anfangs vor einer Herausforderung stand, hat er nie aufgegeben.
Arthur Rudolf Hantzsch, geboren am 7. März 1857 in Dresden, Deutschland, war ein bahnbrechender Chemiker, dessen Beiträge zur organischen Chemie bis heute die Wissenschaft prägen. Seine innovativen Methoden, wegweisenden Theorien und sein Einfluss auf akademische und angewandte Wissenschaften haben sein Vermächtnis in der Chemiegeschichte gefestigt.
Hantzsch wuchs in einer Zeit bedeutender wissenschaftlicher Fortschritte auf, was vermutlich seine Leidenschaft für die Chemie beeinflusste. Er studierte an der Dresdner Polytechnischen Schule und später an der Universität Würzburg, wo er von dem renommierten Chemiker Johannes Wislicenus betreut wurde. Seine akademische Laufbahn gipfelte in der Promotion, die den Grundstein für eine produktive Karriere in Forschung und Lehre legte.
Hantzschs frühe Arbeiten konzentrierten sich auf die Reaktivität und Synthese stickstoffhaltiger Verbindungen. Seine Forschung an Pyridinen, einer Klasse heterocyclischer aromatischer Verbindungen, führte zur Entwicklung des Hantzsch-Widman-Systems. Dieses Nomenklatursystem, das er gemeinsam mit Otto Widman entwickelte, bietet eine systematische Methode zur Benennung heterocyclischer Verbindungen basierend auf Ringgröße und Bestandteilen. Das System ist bis heute ein Eckpfeiler der chemischen Nomenklatur und erleichtert die klare und konsistente Kommunikation in wissenschaftlichen Publikationen.
Eine von Hantzschs bekanntesten Leistungen ist die Hantzsch-Dihydropyridinsynthese, eine Reaktion, die er erstmals 1881 beschrieb. Dieses Verfahren umfasst die Kondensation einer β-Ketocarbonylverbindung, eines Aldehyds und Ammoniak (oder eines primären aliphatischen Amins) zur Herstellung von 1,4-Dihydropyridinen. Diese Verbindungen sind Vorstufen von Pyridinen und haben bedeutende Anwendungen in der medizinischen Chemie.
Heute wird die Hantzsch-Synthese für ihre Nützlichkeit bei der Herstellung von Calciumkanalblockern gefeiert, einer Medikamentenklasse, die für die Behandlung von Herz-Kreislauf-Erkrankungen wie Bluthochdruck und Angina pectoris essenziell ist. Diese direkte Verbindung zur pharmazeutischen Industrie unterstreicht Hantzschs nachhaltigen Einfluss auf die moderne Medizin.
Hantzschs Arbeiten brachten ihm zu Lebzeiten zahlreiche Auszeichnungen ein. Er hatte prestigeträchtige akademische Positionen inne, darunter Professuren an der Universität Würzburg, Leipzig und der Universität Zürich. Seine Wahl in verschiedene wissenschaftliche Akademien und die Verleihung von Ehrendoktortiteln spiegeln die hohe Wertschätzung wider, die ihm von seinen Zeitgenossen entgegengebracht wurde.
Hantzschs Forschung legte grundlegende Prinzipien der organischen Synthese fest und beeinflusste sowohl die theoretische als auch die angewandte Chemie. Seine Beiträge zur heterocyclischen Chemie waren entscheidend für die Entwicklung zahlreicher Arzneimittel. Die Hantzsch-Dihydropyridinsynthese ebnete beispielsweise den Weg für die Entdeckung lebensrettender Medikamente wie Nifedipin, Amlodipin und anderer auf Dihydropyridin basierender Calciumkanalblocker.
Darüber hinaus ermöglichte sein systematischer Ansatz zur chemischen Nomenklatur durch das Hantzsch-Widman-System Chemikern weltweit, komplexe Moleküle präzise und klar zu beschreiben, was die Zusammenarbeit und Innovation über Disziplinen hinweg förderte.
Arthur Hantzsch verstarb am 14. März 1935, doch sein Vermächtnis lebt weiter. Seine bahnbrechenden Methoden und Systeme werden weiterhin in Chemiekursen gelehrt und in Forschungslabors weltweit genutzt. Hantzschs Arbeit exemplifiziert den tiefgreifenden Einfluss, den ein einzelner Wissenschaftler haben kann, indem er die Lücke zwischen theoretischer Erforschung und praktischer Anwendung überbrückt.
Wenn wir über seine Beiträge nachdenken, wird deutlich, dass Hantzsch mehr als nur ein Chemiker war; er war ein Visionär, der das Potenzial seiner Entdeckungen erkannte, Wissenschaft und Gesellschaft zu transformieren. Sein Einfluss wird zweifellos künftige Generationen von Chemikern inspirieren, die Grenzen des Wissens weiter zu verschieben, genau wie er es vor über einem Jahrhundert tat.
Richard F. Heck, ein amerikanischer Chemiker und Nobelpreisträger, wird für seine bahnbrechenden Beiträge zur organischen Chemie gefeiert. Seine Entwicklung der Heck-Reaktion, eines palladiumkatalysierten Kupplungsprozesses, revolutionierte die synthetische Chemie und wurde zu einem Grundpfeiler für die pharmazeutische Entwicklung und Materialwissenschaft. Dieser Text beleuchtet sein Leben, seinen akademischen Werdegang und die nachhaltigen Auswirkungen seiner Arbeit, insbesondere im Hinblick auf Unternehmen wie Chemcon.
Richard F. Heck wurde am 15. August 1931 in Springfield, Massachusetts, geboren. Seine frühe Begeisterung für Wissenschaft und Technologie führte ihn zu einem Chemiestudium an der University of California, Los Angeles (UCLA), das er 1954 mit einer Promotion bei Saul Winstein abschloss. Seine Doktorarbeit legte den Grundstein für seinen späteren Fokus auf die organometallische Chemie.
Nach seiner Promotion forschte Heck an der ETH Zürich, einer der weltweit führenden Institutionen in der Chemie. Später trat er der Hercules Powder Company in Delaware bei, wo er begann, Palladiumchemie zu erforschen. Diese Arbeit bereitete den Weg für seine Anstellung an der University of Delaware, wo seine bedeutendsten Errungenschaften entstanden.
1971 veröffentlichte Heck seine bahnbrechende Arbeit über die palladiumkatalysierte Kupplung von Arylhalogeniden mit Olefinen, die heute als Heck-Reaktion bekannt ist. Diese Reaktion ermöglicht die Bildung von Kohlenstoff-Kohlenstoff-Bindungen mit bemerkenswerter Präzision und Effizienz. Ihre Vielseitigkeit und breite Anwendbarkeit machen sie zu einem unverzichtbaren Werkzeug in der modernen organischen Synthese. Die Heck-Reaktion zeichnet sich durch ihre Fähigkeit aus, die Synthese komplexer organischer Moleküle zu vereinfachen, die Herstellung von Pharmazeutika, einschließlich krebs- und antiviraler Wirkstoffe, zu ermöglichen und fortschrittliche Materialien wie Polymere und Flüssigkristalle zu entwickeln.
Die Bedeutung der Heck-Reaktion für Chemie und Industrie kann nicht überschätzt werden. Sie wird vielfach in der Wirkstoffentwicklung eingesetzt, insbesondere bei der Synthese aktiver pharmazeutischer Wirkstoffe (APIs). Die Effizienz der Reaktion steht im Einklang mit den Prinzipien der Grünen Chemie, da sie Abfälle minimiert und die Umweltbelastung bei der chemischen Herstellung reduziert. Für Unternehmen wie Chemcon, die sich auf GMP-konforme Chemikalien spezialisieren, unterstreicht die Heck-Reaktion die Bedeutung hochreiner Reagenzien und Katalysatoren. Ihre Rolle bei der Optimierung der pharmazeutischen Synthese macht sie zu einem Vorbild für Innovation und Nachhaltigkeit.
Im Jahr 2010 erhielten Richard F. Heck, Akira Suzuki und Ei-ichi Negishi den Nobelpreis für Chemie für „palladiumkatalysierte Kreuzkupplungen in der organischen Synthese“. Diese Auszeichnung betonte die transformative Natur seiner Arbeit, die Chemiker weltweit weiterhin inspiriert. Hecks Vermächtnis reicht über seine wissenschaftlichen Errungenschaften hinaus. Sein Engagement, die Grenzen der Chemie zu erweitern, erinnert an die Bedeutung von Innovation und Zusammenarbeit bei der Lösung komplexer Herausforderungen.
Richard F. Hecks bahnbrechende Arbeit hat einen unauslöschlichen Eindruck in der Chemie hinterlassen, insbesondere in der Pharma- und Materialindustrie. Die Heck-Reaktion zeigt eindrucksvoll, wie Grundlagenforschung technologische Fortschritte vorantreiben und Wege für eine nachhaltige Produktion schaffen kann. Für Chemcon und ähnliche Unternehmen verdeutlichen Hecks Beiträge die entscheidende Rolle hochqualitativer Reagenzien und innovativer Prozesse für Exzellenz in der chemischen Produktion. Sein Vermächtnis inspiriert zu fortwährender Innovation und stellt sicher, dass die chemische Industrie den Anforderungen einer sich schnell wandelnden Welt gerecht wird.
August Wilhelm Hofmann (ab 1888 „von Hofmann“) wurde 1818 in Gießen geboren. Er immatrikulierte sich 1836 an der heutigen Justus-Liebig-Universität in Gießen, zunächst für Rechtswissenschaft, später jedoch für Chemie unter Justus Liebig. 1841 promovierte er unter Liebig mit einer Arbeit über die „Chemische Untersuchung der organischen Basen im Steinkohlenteer „.
In 1845 wurde das „Royal College of Chemistry“ in London mit Hofmann als ersten Direktor gegründet. Nach dem Tod von Prinz Albert ging die Unterstützung der britischen Industrie zurück und Hofmann entschied sich dazu, den Ruf zur Universität Berlin als Professor anzunehmen. Er lehrte anorganische und organische Chemie, schrieb ein Lehrbuch und entwickelte den Hofmann-Zersetzungsapparat.
Im Jahr 1867 gründete er unter anderem mit dem Nobelpreisträger Adolf Bayer die „Deutsche Chemische Gesellschaft“; die Vorgänger Vereinigung zur „Gesellschaft Deutscher Chemiker“ (GDCh).
Die Hofmann Eliminierung ist ein in der Anästhesiologie relevanter Mechanismus in Bezug auf die Inaktivierung bestimmter Muskelrelaxantien.
Rolf Huisgen, geboren am 13. Juni 1920 in Gerolstein, Deutschland, ist ein angesehener deutscher Chemiker, der für seine bahnbrechenden Arbeiten in der organischen Chemie bekannt ist. Sein akademischer Weg begann an der Universität Bonn, wo er Chemie studierte, inspiriert durch das innovative Umfeld und seine Professoren. Nach Abschluss seiner Doktorarbeit unter der Leitung des Nobelpreisträgers Otto Diels im Jahr 1943 setzte Huisgen seine bedeutenden Fortschritte in seinem Fachgebiet fort.
Nach seiner Promotion hatte Huisgen verschiedene akademische Positionen inne und wurde schließlich 1952 Professor an der Universität München. Seine Zeit dort war geprägt von produktiver Forschung und zahlreichen Beiträgen zur organischen Chemie. Huisgens bemerkenswerteste Errungenschaft ist die Entwicklung der 1,3-dipolaren Cycloaddition, allgemein bekannt als Huisgen-Cycloaddition. Diese Reaktion ist ein Eckpfeiler in der Synthese von fünfgliedrigen Heterocyclen und hat die Landschaft der synthetischen Chemie grundlegend verändert.
Unter seinen vielen wissenschaftlichen Leistungen ragt die Huisgen-Pyrrolsynthese hervor. Diese Methode umfasst die Reaktion einer α-Aminosäure mit einer Carbonsäure und einem Alkin zur Bildung eines substituierten Pyrrols. Das Pyrrolringsystem ist ein wesentlicher Bestandteil vieler Naturprodukte und Pharmazeutika, wodurch diese Synthese für die Wirkstoffforschung und -entwicklung von unschätzbarem Wert ist. Huisgens innovativer Ansatz bei Cycloadditionsreaktionen hat den Weg für Fortschritte in den Materialwissenschaften, der medizinischen Chemie und der chemischen Biologie geebnet.
Im Laufe seiner Karriere erhielt Rolf Huisgen zahlreiche Auszeichnungen, darunter die renommierte Adolf-von-Baeyer-Medaille und das Bundesverdienstkreuz. Seine Beiträge haben einen unauslöschlichen Eindruck auf dem Gebiet der organischen Chemie hinterlassen, unzählige Forscher inspiriert und moderne synthetische Methoden geprägt. Das Vermächtnis von Rolf Huisgen beeinflusst weiterhin die wissenschaftliche Gemeinschaft und zeigt den tiefgreifenden Einfluss seiner Arbeit auf die zeitgenössische Chemie.
James Irvin hat mit der Entwicklung der Irvine-Purdie-Methylierungstechnik bedeutende Beiträge zur Chemie geleistet. Seine chemische Laufbahn begann mit einer soliden akademischen Grundlage, die ihn dazu bewog, höhere Bildung anzustreben und letztendlich einen Doktortitel zu erlangen. Während seines Postgraduiertenstudiums entwickelte er zusammen mit seinem Kollegen Purdie diese Methylierungsmethode, die sich seitdem als wertvolles Werkzeug in der synthetischen Chemie etabliert hat.
Diese Technik wird für ihre Effizienz und Präzision bei der Einführung von Methylgruppen in Verbindungen geschätzt, was sie insbesondere in der Pharmazie, Agrochemie und anderen chemischen Industriezweigen vorteilhaft macht. Insbesondere hat sie die Entwicklung von Arzneimitteln beeinflusst, indem sie die Herstellung wirksamerer Pharmazeutika mit weniger Nebenwirkungen ermöglichte und die agrochemischen Produkte durch höhere Sicherheit und Effizienz verbesserte.
Irvins Beiträge gehen über seine wissenschaftlichen Errungenschaften hinaus; er war auch Mentor für viele im Feld und beeinflusste damit die nächste Generation von Chemikern. Die Irvine-Purdie-Methylierung bleibt ein entscheidendes Werkzeug in Chemie und Industrie und unterstreicht Irvins dauerhaften Einfluss auf das Fachgebiet.
Im Bereich der organischen Chemie tritt Eric Jacobsen als eine herausragende Persönlichkeit hervor, bekannt für seine bahnbrechende Forschung auf dem Gebiet der asymmetrischen Katalyse. Seine über Jahrzehnte spannende Karriere ist geprägt von bedeutenden Beiträgen, die die moderne Chemie tiefgreifend beeinflusst haben, insbesondere durch seine Arbeit an der Jacobsen-Epoxidierung.
Geboren in den Vereinigten Staaten, wurde Jacobsens frühes Interesse an der Chemie zum Antrieb für seine Ausbildung in diesem Feld, die in einem Doktortitel von der Harvard University gipfelte. Seine anfänglichen Arbeiten legten den Grundstein für eine Karriere, die von Innovation und Entdeckung geprägt ist.
Nach Abschluss seines Doktorats trat Jacobsen in die Fakultät renommierter Institutionen ein, insbesondere der Harvard University, wo er zahlreiche Auszeichnungen und Ehrungen für seine Beiträge zur Chemie erhalten hat. Diese Anerkennungen spiegeln seine Arbeit in Katalyse und organischer Synthese wider. Seine Zusammenarbeit mit dem Nobelpreisträger Barry Sharpless sticht hervor, indem sie Jacobsens Expertise in der Katalyse mit Sharpless' Wissen in der asymmetrischen Synthese vereint, um die organische Chemie voranzubringen. Diese Partnerschaft unterstreicht Jacobsens Potenzial für zukünftige Nobelpreis-Ehrungen und hebt die Bedeutung von kollaborativer Innovation für den wissenschaftlichen Fortschritt hervor.
Jacobsen ist am bekanntesten für die Jacobsen-Epoxidierung, eine Methode zur enantioselektiven Epoxidierung von unmodifizierten Olefinen unter Verwendung von von seinem Team entwickelten chiralen Katalysatoren. Dieser Durchbruch hat bedeutende Implikationen, insbesondere in der Pharmazie, wo enantiomerenreine Verbindungen entscheidend sind.
Über die Jacobsen-Epoxidierung hinaus umfasst seine Forschung eine breite Palette von Themen innerhalb der asymmetrischen Katalyse, einschließlich der Entwicklung neuer katalytischer Systeme und neuer synthetischer Wege. Jacobsens Forschungsansatz ist definiert durch ein tiefes Verständnis chemischer Mechanismen, innovatives Problemlösen und eine Hingabe an die Weiterentwicklung der organischen Chemie.
Der Nobelpreis für Chemie ehrt Personen, deren wissenschaftliche Leistungen der Menschheit den größten Nutzen gebracht haben. Eric Jacobsens Beiträge, insbesondere in der asymmetrischen Katalyse und der Jacobsen-Epoxidierung, machen ihn zu einem starken Anwärter für diese prestigeträchtige Auszeichnung. Seine Arbeit hat nicht nur die Grenzen des wissenschaftlichen Wissens erweitert, sondern auch praktische Anwendungen in der Arzneimittelentwicklung und -herstellung gefunden, die der Gesellschaft insgesamt zugutekommen.
Jacobsens Weg in der Chemie ist gekennzeichnet durch eine unermüdliche Suche nach Wissen und bahnbrechende Entdeckungen. Seine Beiträge haben einen dauerhaften Stempel auf dem Feld hinterlassen, und die fortlaufende Anerkennung und Erweiterung seiner Arbeit durch die wissenschaftliche Gemeinschaft lassen die wachsende Plausibilität erkennen, dass Jacobsen den Nobelpreis erhält, was eine Karriere feiert, die unser Verständnis der Chemie erheblich vorangebracht hat.
Henry Gilman (1911–1986), ein herausragender amerikanischer Chemiker, wird als der Vater der Organometallchemie gefeiert. Geboren am 1. Dezember 1911 in Boston, Massachusetts, führte Gilmans akademischer Weg zu einem Doktortitel von der Harvard University im Jahr 1935 unter der Anleitung von E.C. Kendall.
Seine illustre Karriere umfasste akademische Positionen an Institutionen wie der Iowa State University, der University of Iowa und dem Iowa State College. Gilmans bahnbrechende Beiträge zur Organometallchemie etablierten ihn als eine Schlüsselfigur auf diesem Gebiet.
Eine seiner bedeutendsten Errungenschaften war die Entwicklung des Gilman-Reagenz – einer Lithium- oder Kupfer-Organocupratverbindung, die in der organischen Synthese weithin zur Bildung von Kohlenstoff-Kohlenstoff-Bindungen verwendet wird. Seine Forschung vertiefte sich in die Synthese, Struktur und Reaktivität von Verbindungen, die Metall-Kohlenstoff-Bindungen enthalten, und trug wesentlich zum Verständnis von Metallierungsreaktionen bei, bei denen ein Metall ein Wasserstoffatom in einem organischen Molekül ersetzt.
Henry Gilmans Vermächtnis erstreckt sich über seine innovativen Methoden hinaus. Er erhielt renommierte Auszeichnungen für seine Arbeit, darunter die Priestley-Medaille, die höchste Auszeichnung der American Chemical Society (ACS). Er wurde in die National Academy of Sciences gewählt und als Mitglied der American Academy of Arts and Sciences anerkannt. Gilman war auch Mitglied der Royal Society of Chemistry.
Die nachhaltige Wirkung von Gilmans Beiträgen spiegelt sich in der fortgesetzten Verwendung des Gilman-Reagenzes und verwandter Reaktionen in der organischen Synthese wider. Seine Hingabe an die Weiterentwicklung der Organometallchemie hat einen bleibenden Eindruck hinterlassen und ihn zu einer geachteten Persönlichkeit in der wissenschaftlichen Gemeinschaft gemacht, die seinen Platz als Pionier auf dem Gebiet der Chemie sichert.
Heinrich Emil Albert Knoevenagel...
..., geboren in Hannover, war ein deutscher Chemiker.
Nach Studien in Hannover und Göttigen promovierte er 1889. Knoevenagel folgte Victor Meyer nach Heidelberg und wurde dort sein Assistent. Er habilitierte sich 1892 in Heidelberg mit dem Thema "Asymmetrischer Kohlenstoff". Emil Knoevenagel arbeitet als Professor an der Universität Heidelberg und beschäftigt sich mit Stickstoff-Heterocyclen-Verbindungen. Die Herstellung von ungesättigten Carbonylverbindungen ist nach ihm als Knoevenagel-Reaktion benannt. Ein besonderes Beispiel für die Aldol-Kondensation.
Ludwig Knorrs Weg in die Annalen der organischen Chemie ist eine Erzählung von intellektueller Suche, Mentorschaft und bahnbrechenden Entdeckungen, die einen bleibenden Eindruck im Fach hinterlassen haben. Geboren am 2. Dezember 1859 in München, Bayern, führten Knorrs frühe akademische Neigungen ihn zunächst zum Studium der Medizin. Doch die Chemie eroberte sein Herz und lenkte seinen Weg hin zu einer der einflussreichsten Persönlichkeiten der organischen Chemie seiner Zeit.
Knorrs akademische Reise nahm eine entscheidende Wendung, als er sich an der Universität Erlangen einschrieb. Hier kam er unter die Fittiche von Emil Fischer, einem Namen, der mit organischer Chemie und deren tiefgreifenden Entwicklungen Ende des 19. und Anfang des 20. Jahrhunderts gleichgesetzt wird. Fischer, der 1902 für seine Arbeiten über Zucker und Purinsynthesen den Nobelpreis für Chemie erhielt, diente als Knorrs Doktorvater. Diese Mentorschaft war entscheidend und stellte Knorr in die vorderste Reihe der Forschung in der organischen Chemie.
Unter Fischers Anleitung begab sich Knorr auf seine Doktorarbeit, die in der Entwicklung der Knorr-Synthese von Pyrrol gipfelte, einem grundlegenden Baustein in der organischen Synthese. Seine Arbeit legte den Grundstein für die Synthese von Pyrrolderivaten, die entscheidend für die Herstellung von Pharmazeutika, Farbstoffen und Agrochemikalien sind. Dieser Erfolg war ein Zeugnis für den Einfluss, den Fischer auf Knorr hatte, und verlieh ihm einen rigorosen Forschungsansatz und einen innovativen Geist, der seine gesamte Karriere prägen würde.
Vielleicht am meisten gefeiert unter Knorrs Beiträgen ist die Entwicklung der Knorr-Chinolinsynthese. Diese elegante chemische Reaktion beinhaltet die Kondensation von Anilin mit β-Ketoesetern zur Bildung von Chinolin oder dessen Derivaten, Verbindungen von bedeutender Wichtigkeit in der pharmazeutischen Industrie aufgrund ihrer therapeutischen Eigenschaften. Die Knorr-Chinolinsynthese hob nicht nur sein Genie in der organischen Synthese hervor, sondern unterstrich auch die Auswirkung seiner Arbeit auf praktische Anwendungen, insbesondere in der Medizin.
Im Laufe seiner Karriere wurde Ludwig Knorr mit zahlreichen Ehrungen ausgezeichnet, die seine zentrale Rolle in der Weiterentwicklung der organischen Chemie widerspiegelten. Doch es war seine Zusammenarbeit und geistige Verwandtschaft mit Emil Fischer, die vielleicht am tiefgreifendsten seinen Ansatz zur Wissenschaft formte. Fischers Mentorschaft bot Knorr eine solide Grundlage in den Prinzipien der organischen Chemie, auf der er aufbaute, um seine bemerkenswerten wissenschaftlichen Beiträge zu leisten.
Knorrs Vermächtnis erstreckt sich über seine chemischen Synthesen hinaus; es liegt in seiner Fähigkeit, theoretische Chemie mit praktischen Anwendungen zu verbinden, was nachfolgende Generationen von Chemikern beeinflusst. Seine Arbeit bleibt ein Eckpfeiler in den Bereichen Pharmazeutika und organische Synthese und verkörpert den anhaltenden Einfluss eines Wissenschaftlers, dessen Streben nach Wissen durch seine Beiträge zum Wohl der Menschheit ergänzt wurde.
Hermann Kolbe wurde 1818 in Elliehausen geboren. Ab 1838 legte der das Abitur in Göttingen ab und startete direkt mit seinem Chemie Studium an der Georg-August-Universität. Ab 1842 wurde er Assistent von Robert Wilhelm Bunsen in Marburg. Seine Promotion beendete im Herbst 1843 mit der Arbeit „Ueber die Produkte der Einwirkung des Chlors auf Schwefelkohlenstoff“. Von 1845 bis 1847 war Kolbe an der University of London Assistent von Lyon Playfair. Während seiner Zeit in London fand er mit Edward Frankland die Darstellungsweise von Carbonsäuren aus Nitrilen. Zur gleichen Zeit fand Kolbe auch eine Darstellung von dimerisierten Alkanen mithilfe von Elektrolyse von Carbonsäuren. Ab 1851 wurde er Nachfolger von Bunsen an der Universität Marburg. Ordentlicher Professor wurde er ab 1865 an der Universität Leipzig. Hier wurde 1868 das „chemische Institut der Universität Leipzig“ nach seinen Plänen gebaut.
Die Kolbe-Schmitt-Reaktion war für die Medizin besonders bedeutsam. Die Salicylsäure besonders deren Derivat die Acetylsalicylsäure (ASS) ist, ist ein unter anderem Fieber und Schmerz lindernder Wirkstoff.
ASS ist seit 1977 auf der Liste der unentbehrlichen Arzneimittel der WHO aufgeführt. Seit Anfang des 20. Jahrhunderts wird der Wirkstoff in diversen Produkten vertrieben.
Nathan Kornblum, ein bedeutender Chemiker des 20. Jahrhunderts, wurde 1914 geboren und hinterließ einen prägenden Einfluss auf die organische Chemie. Sein wissenschaftlicher Weg begann mit einem Studium der Chemie an der Columbia University, wo er seinen Bachelor-Abschluss machte. Anschließend promovierte er an der University of Wisconsin-Madison und begann seine akademische Karriere, die ihn schließlich an die Purdue University führte. Dort wurde er ein angesehener Professor und Forscher, der für seine präzisen und wegweisenden Arbeiten bekannt wurde.
Einer seiner größten Beiträge zur Chemie ist die nach ihm benannte Kornblum-Oxidation, die er in den 1950er Jahren entwickelte. Diese Reaktion hat die organische Synthese nachhaltig beeinflusst und wird bis heute in der Forschung und Industrie angewendet. Die Kornblum-Oxidation ist eine Methode, um primäre Alkylhalogenide in Aldehyde zu überführen, während sekundäre Alkylhalogenide zu Ketonen oxidiert werden. Dabei wird DMSO als Oxidationsmittel verwendet, und die Reaktion findet häufig unter Zugabe von Basen wie Triethylamin statt, um das entstehende Halogenwasserstoffsäure-Derivat zu neutralisieren. Diese Reaktion ist besonders nützlich, da sie unter relativ milden Bedingungen durchgeführt werden kann und eine Alternative zu härteren Oxidationsmitteln darstellt.
Kornblums akademische Leistungen beschränkten sich jedoch nicht nur auf diese Reaktion. Er veröffentlichte im Laufe seiner Karriere zahlreiche wissenschaftliche Artikel und betreute viele Doktoranden, die später selbst bedeutende Wissenschaftler wurden. Seine Arbeit trug wesentlich zur Entwicklung neuer organischer Synthesemethoden bei, die eine breite Anwendung in der Pharmaindustrie und in der Materialforschung fanden.
Trotz seiner beeindruckenden akademischen Errungenschaften war Kornblum für seine Bescheidenheit und seine Leidenschaft bekannt, jungen Wissenschaftlern zu helfen. Er war immer bestrebt, seine Erkenntnisse auf verständliche Weise weiterzugeben, und wurde von seinen Studenten und Kollegen gleichermaßen geschätzt.
Nathan Kornblum verstarb 1978, doch sein wissenschaftliches Erbe lebt weiter. Seine Arbeiten, insbesondere die Kornblum-Oxidation, gehören heute zu den grundlegenden Methoden der organischen Chemie und unterstreichen seinen Platz in der Geschichte der Wissenschaft.
Oleg Grigorjewitsch Kulinkowitsch, ein bedeutender belarussischer Chemiker, hat wesentliche Beiträge zur organischen Chemie geleistet, insbesondere im Bereich der synthetischen Methodenentwicklung. Geboren in der Sowjetunion, entwickelte Kulinkowitsch früh eine Leidenschaft für die Chemie. Sein akademischer Werdegang war geprägt von einem tiefen Verständnis der chemischen Wissenschaften, was ihn dazu führte, sich intensiv mit Forschung und Lehre auseinanderzusetzen. Im Laufe seiner Karriere erlangte er internationale Anerkennung für seine bahnbrechenden Entdeckungen.
Kulinkowitschs wissenschaftliche Laufbahn zeichnete sich durch einen innovativen Ansatz in der organischen Synthese aus, der schließlich zur Entdeckung der nach ihm benannten Kulinkowitsch-Reaktion führte. Diese Reaktion ist eine revolutionäre Methode zur Synthese von Cyclopropanol-Derivaten. Dabei werden Carbonsäureester in Gegenwart eines Titan(IV)-alkoholats als Katalysator mit einer Grignard-Verbindung zu Cyclopropanolen umgewandelt. Die Einfachheit und Effizienz dieser Reaktion machen sie zu einem unverzichtbaren Werkzeug in der organischen Chemie.
Besonders bemerkenswert ist die Kulinkowitsch-Reaktion nicht nur wegen ihrer eleganten Mechanistik, sondern auch aufgrund ihrer breiten Anwendbarkeit in der synthetischen organischen Chemie. Ein bedeutendes Anwendungsgebiet dieser Reaktion ist die Synthese komplexer Moleküle, darunter biologisch wichtige Verbindungen wie Hormone. Cyclopropanole, die Produkte der Kulinkowitsch-Reaktion, sind vielseitige Zwischenprodukte, die weiter modifiziert werden können, um eine Vielzahl biologisch aktiver Verbindungen herzustellen. Dies hat neue Möglichkeiten in der medizinischen Chemie eröffnet, wo die Synthese von Hormonanaloga und anderen pharmazeutischen Wirkstoffen oft die Konstruktion herausfordernder Molekülgerüste erfordert.
Die Nützlichkeit der Kulinkowitsch-Reaktion bei der Hormonsynthese zeigt sich insbesondere in der Herstellung von Steroiden und anderen hormonähnlichen Verbindungen. Die Fähigkeit, Cyclopropan-Ringe effizient zu konstruieren – ein häufiges Strukturmotiv in vielen Naturstoffen und Arzneimitteln – hat Chemikern ein mächtiges Werkzeug an die Hand gegeben, um neue Medikamente zu entwickeln und die Funktionen von Hormonen zu erforschen. Dies hat nicht nur das Feld der organischen Chemie vorangebracht, sondern auch zur Entwicklung neuer Therapien und Arzneimittel beigetragen.
Im Laufe seiner Karriere blieb Oleg Grigorjewitsch Kulinkowitsch stets bestrebt, die Grenzen der chemischen Forschung zu erweitern. Seine Arbeit hat unzählige Chemiker dazu inspiriert, neue Reaktionen zu erforschen und innovative Lösungen für komplexe synthetische Herausforderungen zu entwickeln. Das Vermächtnis seiner gleichnamigen Reaktion prägt das Fachgebiet bis heute und verdeutlicht den bleibenden Einfluss seiner wissenschaftlichen Beiträge.
Neben seinen Forschungsleistungen war Kulinkowitsch auch für seine Rolle als Mentor und seine Zusammenarbeit mit anderen Wissenschaftlern bekannt. Er engagierte sich leidenschaftlich für die Förderung der nächsten Generation von Chemikern und teilte sein Wissen und seine Begeisterung für wissenschaftliche Entdeckungen. Sein Einfluss reichte weit über sein eigenes Labor hinaus, da seine Methoden und Ideen weltweit von Forschern aufgegriffen und weiterentwickelt wurden.
Das Leben und Werk von Oleg Grigorjewitsch Kulinkowitsch sind ein herausragendes Beispiel dafür, welchen tiefgreifenden Einfluss ein einzelner Wissenschaftler auf sein Fachgebiet haben kann. Seine Beiträge zur organischen Chemie, insbesondere die Entwicklung der Kulinkowitsch-Reaktion, haben einen unauslöschlichen Eindruck in der wissenschaftlichen Gemeinschaft hinterlassen. Seine Methoden ermöglichen weiterhin Fortschritte bei der Synthese wichtiger Moleküle, einschließlich Hormonen, und unterstreichen die Bedeutung von Innovation und Kreativität in der wissenschaftlichen Forschung.
Raymond U. Lemieux (1920–2000) war ein bahnbrechender kanadischer organischer Chemiker, dessen wegweisende Arbeiten in der Kohlenhydratchemie das Fachgebiet revolutionierten und den Weg für Fortschritte in der Medizin, Biochemie und Pharmaindustrie ebneten. Seine Beiträge, insbesondere zur Synthese von Glykosiden und zur Aufklärung der Kohlenhydratstruktur, legten das Fundament der modernen Glykowissenschaften.
Geboren in Lac La Biche, Alberta, entwickelte Lemieux früh eine Leidenschaft für Chemie, die ihn zum Studium an der University of Alberta führte. Er promovierte an der McGill University unter der Betreuung von Carl Niemann mit dem Schwerpunkt Kohlenhydratchemie—einem damals noch wenig erforschten Gebiet.
Eine seiner bedeutendsten Errungenschaften war die Synthese von Glykosiden. 1953 gelang es ihm und seinem Team erstmals, Saccharose künstlich herzustellen, womit er eine der ersten komplexen Zuckerverbindungen synthetisierte. Diese Leistung vertiefte nicht nur das Verständnis von Zuckerstrukturen, sondern hatte auch weitreichende Auswirkungen auf die pharmazeutische und biotechnologische Forschung.
Lemieux' Forschung zur Glykosylierung—dem Prozess der Anheftung von Zuckermolekülen an andere Biomoleküle—führte zu Innovationen in der Antibiotikaentwicklung, bei Blutgruppenantigenen und in der Impfstoffherstellung. Seine Arbeiten hatten direkten Einfluss auf die Produktion von Heparin und anderen kohlenhydratbasierten Arzneimitteln, die essenziell für die Antikoagulationstherapie und die Immunmodulation sind.
Eine weitere bemerkenswerte Entdeckung war die Entwicklung der Lemieux-Johnson-Oxidation, einer Methode zur oxidativen Spaltung von Alkenen in Carbonylverbindungen unter Verwendung von Osmiumtetroxid und Periodat. Diese Reaktion wird bis heute häufig in der organischen Synthese und pharmazeutischen Forschung eingesetzt und hat die Wirkstoffentwicklung nachhaltig beeinflusst. Sein bahnbrechendes Werk hat die moderne pharmazeutische Wissenschaft maßgeblich geprägt, insbesondere bei der Synthese komplexer Kohlenhydrate, die in Impfstoffen, Therapeutika und diagnostischen Verfahren Verwendung finden.
Über seine akademischen Errungenschaften hinaus spielte Lemieux eine zentrale Rolle in der Pharmaindustrie. Er gründete das Biotechnologieunternehmen Chembiomed, das sich auf kohlenhydratbasierte Arzneimittel spezialisierte. Darüber hinaus hatten seine Erkenntnisse zur biologischen Funktion von Kohlenhydraten tiefgreifende Auswirkungen auf die Immunologie und die Erforschung von Krankheiten.
Für seine Verdienste um die Chemie erhielt Lemieux zahlreiche Auszeichnungen, darunter den renommierten Wolf-Preis für Chemie und die Royal Medal der Royal Society of London. Seine Arbeiten etablierten Kanada als führenden Standort für Kohlenhydratchemie und schufen die Grundlage für zukünftige Entdeckungen in der Glykobiologie und medizinischen Chemie.
Das Vermächtnis von Raymond Lemieux beeinflusst die wissenschaftliche Forschung bis heute und unterstreicht die zentrale Rolle von Kohlenhydraten in den Lebenswissenschaften und der Arzneimittelentwicklung. Seine bahnbrechenden Forschungen bleiben ein Grundpfeiler der modernen Chemie und zeigen, dass selbst die komplexesten Moleküle verstanden und für das Wohl der Menschheit nutzbar gemacht werden können.
Wilhelm Clemens Lossen wurde am 8. Mai 1838 in Kreuznach, heute bekannt als Bad Kreuznach in Deutschland, geboren. Seine akademische Laufbahn in der Chemie umfasste bedeutende Mentoren; er war insbesondere Assistent bei Karl Weltzien in Karlsruhe und bei Wilhelm Heinrich Heintz in Halle. Seine Karriere an der Universität entwickelte sich weiter, als er die Rolle eines außerordentlichen Professors an der Universität Heidelberg übernahm und später zum ordentlichen Professor für Chemie an der Universität Königsberg ernannt wurde.
Lossen ist vielleicht am besten bekannt für die nach ihm benannte Lossen-Umlagerung, eine organisch-chemische Reaktion, bei der Hydroxamsäuren mit einem Entwässerungsmittel in Isocyanate umgewandelt werden. Diese Reaktion wird wegen ihrer Bedeutung für die Synthese verschiedener organischer Verbindungen, insbesondere in der pharmazeutischen Industrie, wo sie eine entscheidende Rolle bei der Entwicklung neuer Arzneimittel spielt, weitgehend anerkannt.
Während seiner gesamten Karriere war Lossen tief in der akademischen und wissenschaftlichen Gemeinschaft engagiert und trug durch Lehre und Forschung umfangreich bei. Sein Ansatz in Bildung und Mentorship hinterließ einen nachhaltigen Einfluss auf seine Studenten und Kollegen und förderte ein Vermächtnis der Untersuchung und Entdeckung.
Wilhelm Clemens Lossen verstarb am 29. Oktober 1906 in Aachen. Seine Beiträge zur Chemie werden weiterhin gefeiert und bleiben für verschiedene wissenschaftliche Anwendungen heute integral.
Carl Ulrich Franz Mannich wurde 1877 in Breslau geboren. Er studierte ab 1898 Pharmazie in Marburg und Berlin. In 1903 promovierte er in Basel und habilitierte 1907 in Berlin. Von 1911 bis 1917 lehrte er pharmazeutische Chemie in Göttingen. Ab 1920 ging er nach Frankfurt am Main. Danach war Mannich bis 1943 Ordinarius für pharmazeutische Chemie an der Friedrich-Wilhelms-Universität Berlin und gleichzeitig Direktor des pharmazeutischen Instituts. Ab 1946 übernahm er den Lehrstuhl für pharmazeutische Chemie am heutigen Karlsruher Institut für Technologie.
Von 1932 bis 1934 war er der Präsident der „Deutschen Pharmazeutischen Gesellschaft“, welche seit 1959 die Carl-Mannich-Medallie für „hervorragende Leistungen auf dem Gebiet der wissenschaftlichen Pharmazie“ verleiht.
Die Mannich Reaktion findet Anwendung in der Synthese von Naturstoffen, der Herstellung von Arznei- und Pflanzenschutzstoffe sowie der Lack- und Polymerchemie.
Wir bei ChemCon haben als CDMO über 25 Jahre Erfahrung mit der Entwicklung und Herstellung von Arzneistoffen (API) unter höchsten GMP Bedingungen. Unter anderem sind das Wirkstoffe mit Anwendung in der Krebstherapie, Augenheilkunde und gegen seltene Krankheiten (orphan diseases).
Neben der Auftragsentwicklung hat ChemCon ein namhaftes Labor zur Auftragsanalytik aufbauen können welches nach GMP- und ICH-Richtlinien, sowie Arzneibuch, Ph. Eur. etc. fungiert.
Seit einigen Jahren wird auch die Substanzklasse der Polymere, insbesondere die Polyethylenimine (PEI) und die Polyoxazoline (PxOx), in unseren Laboren hergestellt. In der pharmazeutischen Industrie können diese als Reagenz zur Trennung von Nukleinsäuren eingesetzt werden. PEIs werden außerdem als Transfektionsmittel verwendet. Um als Hilfstoffe in Medikamenten eingesetzt zu werden müssen sie nach GMP hergestellt werden. Hierbei hat ChemCon die größte Erfahrung.
John E. McMurry ist ein renommierter amerikanischer Chemiker, der für seine bedeutenden Beiträge zur organischen Chemie bekannt ist. Geboren im Jahr 1942, widmete sich McMurry intensiv der Entwicklung synthetischer Methoden. Nach seiner Promotion an der Columbia University unter der Leitung von Gilbert Stork begann er eine erfolgreiche Karriere in Forschung und Lehre. Als Professor an der Cornell University erlangte McMurry nicht nur durch seine bahnbrechenden Forschungsarbeiten Anerkennung, sondern auch durch seine einflussreichen Lehrbücher, die bis heute die Vermittlung der organischen Chemie prägen.
Eine seiner herausragendsten wissenschaftlichen Leistungen ist die Entwicklung der McMurry-Reaktion, einer effektiven Methode zur Bildung von Kohlenstoff-Kohlenstoff-Doppelbindungen. Diese Reaktion ermöglicht die reduktive Kupplung von zwei Carbonylverbindungen – Aldehyden oder Ketonen – unter Verwendung von niedervalenten Titanverbindungen. Die entstehenden Alkene sind wertvolle Zwischenprodukte in der organischen Synthese und bieten eine vielseitige Möglichkeit zur Herstellung komplexer Moleküle. Aufgrund ihrer Effizienz und ihrer Fähigkeit, anspruchsvolle molekulare Strukturen zu erzeugen, ist die McMurry-Reaktion zu einer zentralen Technik der modernen organischen Chemie geworden.
Über ihre akademische Bedeutung hinaus spielt die McMurry-Reaktion eine zentrale Rolle in der pharmazeutischen Industrie. Sie ermöglicht die Synthese strukturell komplexer Verbindungen, einschließlich biologisch aktiver Moleküle, die für die Arzneimittelentwicklung von entscheidender Bedeutung sind. Diese Methode ist besonders nützlich bei der Herstellung einzigartiger chemischer Gerüste und der Erkundung neuer Wirkstoffkandidaten. Durch die gezielte Konstruktion komplexer Kohlenstoffgerüste eröffnet die McMurry-Reaktion neue Wege zur Entwicklung innovativer pharmazeutischer Wirkstoffe und fortschrittlicher Materialien.
Bei Chemcon gehört die McMurry-Reaktion zu den fortgeschrittenen Techniken, die in kundenspezifischen Syntheseprojekten eingesetzt werden. Die präzise Modifikation von Carbonylverbindungen passt zu Chemcons Expertise in der Bereitstellung spezialisierter chemischer Lösungen. Ob in der frühen Forschungsphase oder in der großtechnischen Produktion – der Einsatz solcher Methoden ermöglicht es Chemcon, maßgeschneiderte Verbindungen zu liefern, die höchsten Qualitäts- und regulatorischen Standards entsprechen. Diese Flexibilität ist besonders wertvoll bei der Entwicklung von Wirkstoffen (APIs) und anderen essenziellen Materialien, bei denen eine individualisierte chemische Synthese erforderlich ist. Durch die Nutzung von Reaktionen wie der McMurry-Reaktion unterstützt Chemcon weiterhin Innovation und Effizienz in der Pharma- und Chemieindustrie und bietet seinen Kunden die Möglichkeit, komplexe chemische Konzepte in greifbare Produkte umzusetzen.
Arthur Michael...
...war ein US-amerikanischer Chemiker, der nie seinen Universitätsabschluss machte. Sein Wissen über Chemie eignete er sich durch lokale Lehrer in seinem Privatlabor an. Aufgrund einer Krankheit war es ihm nicht möglich ein Studium in Harvard zu absolvieren. Weiteres Wissen erlang er durch Besuche von bekannten Chemikern auf einer Europareise. Am Tufts College lernte er seine Frau kennen und arbeitete als Professor für Chemie. 1912 ging er an die Harvard University, an der er bis 1936 als Professor ohne Vorlesungspflicht wirkte. Heutzutage ist Arthur Michael hauptsächlich für die nach ihm benannte Michael Addition bekannt.
Oyo Mitsunobu, ein angesehener japanischer Chemiker, ist bekannt für seine bedeutenden Beiträge zur organischen Chemie, insbesondere durch die nach ihm benannte Mitsunobu-Reaktion. Geboren 1934 in Japan, war Mitsunobus frühes Leben von einem ausgeprägten Interesse an Wissenschaft und einer unerschütterlichen Hingabe an seine Studien geprägt. Er absolvierte sein Hochschulstudium an der Universität Tokio, wo er schließlich seinen Doktortitel in organischer Chemie erlangte. Seine akademische Laufbahn war geprägt von einem intensiven Fokus auf die Entwicklung innovativer chemischer Reaktionen, die später sein Vermächtnis in der wissenschaftlichen Gemeinschaft festigen sollten.
Mitsunobus bedeutendste Errungenschaft ist die Entwicklung der Mitsunobu-Reaktion, ein transformativer Prozess in der organischen Synthese, der die Umwandlung von Alkoholen in verschiedene andere funktionelle Gruppen, einschließlich Ester, Ether, Amine und Thioether, ermöglicht. Diese Reaktion verwendet spezifische Reagenzien wie Diethylazodicarboxylat (DEAD), Diisopropylazodicarboxylat (DIAD) oder tert-Butylazodicarboxylat (TMAD), die die Substitution der Hydroxygruppe durch Nukleophile erleichtern. Ein besonderes Merkmal der Mitsunobu-Reaktion ist ihre Fähigkeit, eine Inversion der Konfiguration an stereogenen Zentren zu induzieren. Das bedeutet, dass sekundäre Alkohole, wenn sie den Reaktionsbedingungen unterworfen werden, eine stereochemische Inversion erfahren, was diese Reaktion besonders wertvoll für die Synthese enantiomerenreiner Verbindungen macht.
Die Mitsunobu-Reaktion ist jedoch nicht ohne Nachteile. Eine wesentliche Kritik ist ihre schlechte Atomökonomie. Die Reaktion erzeugt eine beträchtliche Menge an Nebenprodukten, die die Reinigung erschweren und die Gesamteffizienz verringern können. Trotz dieser Einschränkung bleibt die Reaktion wegen ihrer Vielseitigkeit und ihrer Fähigkeit, Kohlenstoff-Stickstoff- und Kohlenstoff-Sauerstoff-Bindungen zu bilden, besonders im Hinblick auf die Umwandlung von Hydroxygruppen in Aminogruppen, sehr geschätzt. Diese Umwandlung ist besonders nützlich in der pharmazeutischen Synthese, wo präzise Modifikationen von Molekülstrukturen oft erforderlich sind.
Oyo Mitsunobus Einfluss auf die heutige Wissenschaft ist tiefgreifend. Die Mitsunobu-Reaktion bildet die Grundlage für zahlreiche Patente und wissenschaftliche Publikationen und spiegelt ihre weit verbreitete Anwendung sowohl in der akademischen Forschung als auch in industriellen Prozessen wider. Die Nützlichkeit der Reaktion bei der Erstellung komplexer Moleküle hat sie zu einem festen Bestandteil im Werkzeugkasten synthetischer Chemiker weltweit gemacht. Ihre Anwendung reicht über einfache Transformationen hinaus und beeinflusst die Entwicklung neuer Methoden sowie die Synthese komplexer Naturprodukte und Pharmazeutika.
Im Laufe seiner Karriere erhielt Mitsunobu mehrere Auszeichnungen für seine Arbeit, was seinen Einfluss auf das Gebiet der organischen Chemie unterstreicht. Sein innovativer Ansatz und die anschließende Entwicklung der Mitsunobu-Reaktion haben unzählige Chemiker inspiriert, neue Grenzen in der chemischen Synthese zu erkunden. Die anhaltende Relevanz der Reaktion in der modernen Chemie ist ein Zeugnis für Mitsunobus Einfallsreichtum und sein dauerhaftes Vermächtnis in der wissenschaftlichen Gemeinschaft.
Ei-ichi Negishi war eine der herausragendsten Persönlichkeiten auf dem Gebiet der Chemie, bekannt vor allem für die Entwicklung der Negishi-Kupplung, einer Methode, die weitreichend in der Synthese komplexer organischer Verbindungen verwendet wird. Geboren 1935 in Changchun, China, zog Negishi mit seiner Familie am Ende des Zweiten Weltkriegs nach Japan. Dort setzte er seine Ausbildung fort und erlangte 1958 seinen Bachelor-Abschluss an der Universität Tokio.
Negishis Weg zur weltweiten Anerkennung begann, als er in die Vereinigten Staaten ging, um sein Studium fortzusetzen. Er promovierte 1963 in Chemie an der University of Pennsylvania unter der Leitung des berühmten Chemikers Allan R. Day. Später schloss er sich der Gruppe eines weiteren renommierten Chemikers, Herbert C. Brown, an der Purdue University als Postdoktorand an. Diese Verbindung war entscheidend, da Browns Arbeit über Organoborane ihm später einen Nobelpreis einbringen würde und Negishis eigene Forschungsrichtung tiefgehend beeinflusste.
Negishi verbrachte den Großteil seiner Karriere an der Purdue University, wo er 1972 als Assistenzprofessor begann und 1979 zum ordentlichen Professor befördert wurde. Sein Forschungsschwerpunkt lag auf der Entwicklung von Methoden zur einfachen und effizienten Verknüpfung von Kohlenstoffatomen, einem grundlegenden Aspekt der organischen Synthese. Der bedeutendste Durchbruch in Negishis Karriere war die Entwicklung der Negishi-Kupplung Ende der 1970er Jahre. Diese leistungsfähige chemische Reaktion beinhaltet die Kreuzkupplung von Organzinkverbindungen mit Aryl- oder Alkenylhaliden, katalysiert durch Palladium oder Nickel. Die Eleganz und Effizienz dieser Reaktion machten sie zu einem wertvollen Werkzeug für den Aufbau komplexer, multifunktionaler organischer Verbindungen, einschließlich Pharmazeutika, Naturstoffen und fortschrittlichen Materialien.
Die Bedeutung von Negishis Arbeit wurde 2010 anerkannt, als ihm zusammen mit Richard F. Heck und Akira Suzuki der Nobelpreis für Chemie verliehen wurde. Das Trio wurde für seine Beiträge zur Entwicklung von palladiumkatalysierten Kreuzkupplungen in der organischen Synthese geehrt, die die Art und Weise, wie Chemiker komplexe Moleküle aufbauen, revolutioniert haben. Das Nobelpreiskomitee hob insbesondere die breite Anwendbarkeit dieser Methoden sowohl im akademischen als auch im industriellen Umfeld hervor, da sie die Herstellung anspruchsvoller chemischer Produkte praktischer und umweltfreundlicher machen.
Während seiner gesamten Karriere war Negishi nicht nur ein brillanter Chemiker, sondern auch ein engagierter Mentor und Lehrer. Er war leidenschaftlich daran interessiert, die nächste Generation von Wissenschaftlern zu inspirieren, und betonte oft die Bedeutung von Neugier, Ausdauer und grundlegendem Verständnis in der wissenschaftlichen Forschung. Seine Lehren und Philosophien haben bei vielen seiner Studenten und Kollegen einen bleibenden Eindruck hinterlassen.
Ei-ichi Negishis Beiträge zur Chemie sind tiefgreifend und reichen über das Labor hinaus, um verschiedene Industrien, einschließlich der Pharmaindustrie und der Materialwissenschaft, zu beeinflussen. Seine Arbeit veranschaulicht die Kraft chemischer Innovationen bei der Lösung komplexer Probleme und der Verbesserung des Lebens. Das Erbe seiner wissenschaftlichen Leistungen und sein Engagement für die Bildung inspirieren und beeinflussen auch heute noch das Fachgebiet der Chemie.
Ronald George Wreyford Norrish, geboren am 9. November 1897 in Cambridge, England, war für ein Leben voller akademischer Exzellenz bestimmt. Sein Vater, George Norrish, war Apotheker, ein Beruf, der Präzision und analytisches Denken erfordert—Eigenschaften, die der junge Ronald in seine wissenschaftlichen Bestrebungen einbringen würde. Die intellektuelle Umgebung von Cambridge spielte zweifellos eine entscheidende Rolle bei der Gestaltung von Norrishs Zukunft und bot ihm Zugang zu einigen der besten Bildungseinrichtungen der Welt.
Norrishs akademische Laufbahn begann an der renommierten Perse School in Cambridge, gefolgt von seinem Studium am Emmanuel College, University of Cambridge. Seine Ausbildung wurde kurzzeitig durch seinen Dienst im Ersten Weltkrieg unterbrochen, wo er verwundet wurde. Nach dem Krieg kehrte er nach Cambridge zurück und schloss 1921 sein Chemiestudium ab.
Norrishs Brillanz auf dem Gebiet der Chemie wurde schnell deutlich. Er wurde 1925 zum Dozenten in Cambridge ernannt und wurde schließlich Professor für Physikalische Chemie. Seine Arbeit war maßgeblich für das Verständnis der chemischen Kinetik und der Photochemie. Norrishs Forschung war geprägt von einer tiefen Neugier auf die Mechanismen chemischer Reaktionen und wie Licht diese Prozesse beeinflussen kann.
Norrishs bedeutendste Beiträge liegen im Bereich der Photochemie, dem Studium von chemischen Reaktionen, die durch die Absorption von Licht entstehen. Er erforschte die photochemische Zersetzung von Carbonylverbindungen, einer Klasse organischer Verbindungen, die eine Kohlenstoff-Sauerstoff-Doppelbindung enthalten. Seine Arbeit auf diesem Gebiet legte den Grundstein für einen Großteil der modernen Photochemie.
Eine von Norrishs wichtigsten Entdeckungen war die Norrish-Reaktion, die die photochemische Spaltung von Carbonylverbindungen beschreibt. Durch die Absorption eines Photons wird die Carbonylgruppe in einen Singulett-Zustand angeregt. Dieser angeregte Zustand kann entweder einen Triplett-Zustand bilden oder direkt eine Bindungsspaltung durchführen, um freie Radikale zu erzeugen. Diese freien Radikale nehmen dann an verschiedenen Folgereaktionen teil und bilden die Grundlage für zahlreiche photochemische Prozesse in der organischen Chemie.
Ein weiteres wichtiges Phänomen, das mit Norrish verbunden ist, ist der Trommsdorff-Norrish-Effekt, der sich auf die Auto-Beschleunigung von Polymerisationsreaktionen bezieht. Wenn bestimmte Polymere Licht ausgesetzt werden, steigt die Polymerisationsrate aufgrund der Bildung reaktiver Spezies schnell an. Dieser Effekt ist jedoch nicht auf lichtinduzierte Polymerisationen beschränkt; er kann auch bei thermisch initiierten Polymerisationen und anderen Arten von Kettenreaktionen auftreten. Dieser Effekt ist besonders bedeutend bei der Herstellung synthetischer Polymere und hat industrielle Anwendungen zur Schaffung von Materialien mit spezifischen Eigenschaften.
Ronald Norrishs bahnbrechende Arbeit blieb nicht unbemerkt. 1967 wurde ihm der Nobelpreis für Chemie verliehen, den er sich mit seinem Kollegen George Porter und dem deutschen Chemiker Manfred Eigen teilte. Das Nobelkomitee würdigte ihre gemeinsamen Bemühungen um das Studium extrem schneller chemischer Reaktionen, die in Nanosekunden gemessen werden. Besonders bemerkenswert war die Entwicklung der Flash-Photolyse-Technik durch Norrish und Porter. Diese Methode ermöglichte es Chemikern, die Zwischenstufen photochemischer Reaktionen zu beobachten und revolutionierte das Verständnis von Reaktionsmechanismen.
Ronald George Wreyford Norrish verstarb am 7. Juni 1978 und hinterließ ein Vermächtnis wissenschaftlicher Innovation und Entdeckung. Seine Arbeit beeinflusst noch heute Chemiker, insbesondere in den Bereichen der Physikalischen Chemie und der Photochemie. Die Norrish-Reaktion und der Trommsdorff-Norrish-Effekt bleiben wesentliche Bestandteile des Verständnisses chemischer Prozesse, sowohl in der akademischen Forschung als auch in industriellen Anwendungen. Norrishs Leben ist ein Zeugnis für die Kraft der Neugier und des Durchhaltevermögens in der wissenschaftlichen Forschung. Seine Beiträge haben den Weg für zukünftige Generationen von Chemikern geebnet, um den komplexen Tanz der Moleküle unter dem Einfluss von Licht zu erforschen und die Grenzen unseres Wissens über die chemische Welt zu erweitern.
Tamejiro Hiyama ist ein angesehener japanischer Chemiker, dessen bahnbrechende Beiträge zur organischen und metallorganischen Chemie einen tiefgreifenden Einfluss auf moderne synthetische Methoden, insbesondere in der pharmazeutischen Chemie, hatten. Seine Arbeiten haben nicht nur unser Verständnis katalytischer Prozesse erweitert, sondern auch innovative Werkzeuge für die Konstruktion komplexer molekularer Strukturen bereitgestellt.
Geboren 1947 in Japan, zeigte Tamejiro Hiyama schon früh Interesse an Naturwissenschaften und Chemie. Sein Chemiestudium absolvierte er an der renommierten Universität Kyōto, wo er später auch seine Promotion erlangte. 1974 schloss er diese unter der Anleitung bedeutender Chemiker ab, die seine frühen Arbeiten zur metallorganischen Chemie maßgeblich prägten.
Nach seiner Promotion sammelte Hiyama wertvolle internationale Erfahrungen als Postdoktorand an der Purdue University in den Vereinigten Staaten. Dort vertiefte er sein Fachwissen in der synthetischen Chemie und Katalyse. Diese internationale Perspektive prägte seine spätere Forschungsrichtung nachhaltig.
Zurück in Japan begann Hiyama eine beeindruckende akademische Karriere. Er hatte Lehrstühle an der Universität Kyōto und später an der Universität Nagoya inne, zwei führenden Zentren für chemische Forschung. Im Laufe der Jahrzehnte etablierte er sich als führende Persönlichkeit der metallorganischen Chemie, bildete zahlreiche Studenten aus und förderte internationale Kooperationen.
Hiyamas wissenschaftliche Beiträge sind sowohl vielfältig als auch einflussreich. Zu seinen bedeutendsten Leistungen zählt die Entwicklung der Nozaki-Hiyama-Kishi-Reaktion (NHK-Reaktion), einer Methode zur Kohlenstoff-Kohlenstoff-Bindungsknüpfung. Diese Reaktion, die er gemeinsam mit Hideo Nozaki und Yoshito Kishi entwickelte, ermöglicht die Kupplung von Alkyl- oder Allylhalogeniden mit Aldehyden unter Einsatz von Chrom- oder Nickelkatalysatoren. Diese Methode hat sich zu einem Grundpfeiler der synthetischen organischen Chemie entwickelt und ermöglicht die effiziente Herstellung von sekundären und tertiären Alkoholen.
Die NHK-Reaktion wird besonders für ihre Fähigkeit geschätzt, komplexe Kohlenstoffgerüste zu erzeugen, wie sie oft in Naturstoffen und pharmazeutischen Verbindungen vorkommen. Ihre Vielseitigkeit und Effizienz haben sie zu einem unverzichtbaren Werkzeug für synthetische Chemiker weltweit gemacht.
Hiyamas Beiträge gehen über die Grundlagenforschung hinaus und finden Anwendung in der Wirkstoffforschung und -entwicklung. Die NHK-Reaktion war beispielsweise entscheidend für die Synthese biologisch aktiver Moleküle, einschließlich Naturstoffen mit therapeutischem Potenzial. Durch die Möglichkeit, präzise und effiziente Bindungen zu knüpfen, haben Hiyamas Methoden die Synthese komplexer pharmazeutischer Verbindungen vereinfacht, Kosten reduziert und die Skalierbarkeit verbessert.
Darüber hinaus hat Hiyama intensiv an siliziumbasierten Reagenzien gearbeitet und Protokolle entwickelt, die die Selektivität und Effizienz organischer Transformationen verbessert haben. Diese Innovationen haben seinen Einfluss in der medizinischen Chemie weiter gefestigt, wo Präzision und Anpassungsfähigkeit von entscheidender Bedeutung sind.
Tamejiro Hiyamas Beiträge zur Chemie wurden vielfach anerkannt. Er erhielt zahlreiche Auszeichnungen, darunter den Preis der Chemischen Gesellschaft Japans und den Humboldt-Forschungspreis, die seine internationale Bedeutung unterstreichen. Seine Hinterlassenschaft lebt jedoch nicht nur durch die Auszeichnungen weiter, sondern auch durch die zahlreichen Chemiker, die er ausgebildet hat, und die anhaltende Relevanz seiner Methoden.
Heute bleibt Tamejiro Hiyama eine inspirierende Figur in der globalen chemischen Gemeinschaft. Seine Arbeit zeigt eindrucksvoll, wie grundlegende Forschung Innovationen in praktischen Anwendungen vorantreiben kann, insbesondere in so wichtigen Bereichen wie der pharmazeutischen Chemie. Während neue Generationen von Chemikern auf seinen Grundlagen aufbauen, wird Hiyamas Einfluss zweifellos die Zukunft von Wissenschaft und Medizin weiter prägen.
Larry E. Overman, ein herausragender amerikanischer Chemiker, ist bekannt für seine Beiträge zur organischen Chemie, insbesondere für die Overman-Umlagerung. Seine bahnbrechenden Arbeiten haben die synthetische Chemie tiefgreifend beeinflusst, besonders in der Synthese komplexer Naturprodukte und pharmazeutischer Verbindungen.
Geboren 1943 in Chicago, Illinois, zeigte Overman schon früh ein Interesse an den Naturwissenschaften, was den Weg für seine akademische Laufbahn ebnete. Er erwarb seinen Bachelor of Science in Chemie am Earlham College, einem College der freien Künste, das für seine Schwerpunktsetzung auf Forschung im Grundstudium bekannt ist. Anschließend promovierte Overman an der University of Wisconsin-Madison, wo er unter der Leitung von Howard E. Zimmerman arbeitete. Seine Doktorarbeit konzentrierte sich auf photochemische Reaktionen, ein Thema, das in seiner gesamten Karriere wiederkehren sollte.
Nach seinem Doktorabschluss nahm Overman eine Stelle an der University of California, Irvine, an, wo er den Großteil seiner akademischen Karriere verbrachte. Hier machte er bedeutende Fortschritte in der organischen Synthese und entwickelte neue Methoden, die zu wesentlichen Werkzeugen für Chemiker weltweit geworden sind. Unter seinen vielen Errungenschaften sticht die Overman-Umlagerung hervor. Diese in den 1970er Jahren entwickelte Reaktion ermöglicht die Umwandlung von allylischen Alkoholen in allylische Amine unter Verwendung von Trichloracetimidat als Schlüsselreagenz. Die Overman-Umlagerung ist besonders dafür bekannt, effizient chirale Aminstrukturen zu erzeugen, die in der Synthese vieler biologisch aktiver Moleküle zentral sind.
Die Auswirkungen der Overman-Umlagerung gehen über die theoretische Chemie hinaus. Sie findet praktische Anwendung in der Synthese komplexer Moleküle, insbesondere in der pharmazeutischen Industrie. Beispielsweise wurde sie bei der Entwicklung von Polyallylamin-Verbindungen eingesetzt, die für die Herstellung leistungsfähiger Polymere unerlässlich sind. Diese Polymere haben verschiedene industrielle Anwendungen, einschließlich der Wasseraufbereitung und der Verbesserung der Papierfestigkeit.
Darüber hinaus spielte die Overman-Umlagerung eine entscheidende Rolle bei der Synthese von Sevelamer, einem Arzneimittel zur Bindung von Phosphat, das zur Behandlung von Hyperphosphatämie bei Patienten mit chronischer Nierenerkrankung verwendet wird. Die Synthese von Sevelamer verdeutlicht die praktischen gesundheitlichen Auswirkungen von Overmans Arbeit und zeigt, wie grundlegende chemische Reaktionen zu bedeutenden Fortschritten in der Medizin führen können.
Im Laufe seiner Karriere wurde Overman mit zahlreichen Auszeichnungen und Ehrungen anerkannt, die seinen Status als führende Persönlichkeit in der Chemie widerspiegeln. Sein Einfluss zeigt sich auch in seiner Rolle als Mentor für junge Chemiker, von denen viele bedeutende eigene Beiträge zur Wissenschaft geleistet haben.
Zusammenfassend lässt sich sagen, dass Larry E. Overmans Werk exemplarisch dafür steht, wie tiefgreifendes theoretisches Wissen in Verbindung mit einem Engagement für praktische Anwendungen zu Fortschritten führen kann, die weit über das Labor hinausgehen. Seine Entwicklung der Overman-Umlagerung hat nicht nur das Werkzeugset organischer Chemiker erweitert, sondern auch erhebliche Fortschritte in der Entwicklung von Pharmazeutika und Industriematerialien ermöglicht. Sein Erbe ist ein Zeugnis für die Kraft der Chemie, komplexe Probleme zu lösen und das menschliche Leben zu verbessern.
Emanuele Paternò war eine bedeutende Figur in der Chemie, deren Beiträge bis heute in der wissenschaftlichen und pharmazeutischen Gemeinschaft nachwirken. Geboren 1847 in Palermo, Italien, wuchs Paternò in einer Zeit auf, die von wissenschaftlicher Neugier und technologischen Fortschritten geprägt war. Schon früh zeigte er eine natürliche Begabung für die Naturwissenschaften, was ihn auf eine Karriere vorbereitete, die das Fachgebiet nachhaltig beeinflussen sollte. Nach seinem Studium, das ihn unter die Anleitung bedeutender Chemiker seiner Zeit führte, entwickelte er einen gründlichen und neugierigen Forschungsansatz, den er über seine gesamte Karriere hinweg beibehielt. Seine akademische Laufbahn führte ihn quer durch Europa, wo er Wissen aufnahm und zur wachsenden Sammlung chemischen Wissens beitrug – ein Weg, der schließlich in der Entdeckung der nach ihm benannten Paternò-Büchi-Reaktion gipfelte.
Diese photochemische Reaktion, die als Paternò-Büchi-Reaktion bekannt ist, stellt einen Meilenstein seiner Arbeit dar und bleibt bis heute ein grundlegendes Werkzeug in der organischen Synthese. In dieser Reaktion reagieren Carbonylverbindungen unter Lichteinfluss mit Alkenen und bilden dabei einen viergliedrigen Oxetan-Ring. Diese Entdeckung war revolutionär, da sie das Potenzial der Photochemie zur Erzeugung komplexer Molekülstrukturen aufzeigte – eine Möglichkeit, die damals weitgehend unerforscht war. Indem er die Energie des Lichts nutzte, um chemische Umwandlungen zu ermöglichen, zeigte Paternò, wie Reaktionen, die unter traditionellen Bedingungen kaum durchführbar schienen, tatsächlich machbar sind. Der von ihm entwickelte [2+2]-Cycloadditions-Mechanismus eröffnete nicht nur neue Wege für die Synthese, sondern legte auch den Grundstein für zukünftige Fortschritte in der organischen Photochemie. Diese bahnbrechende Idee inspirierte weiterführende Forschungen darüber, wie Licht genutzt werden kann, um chemische Reaktionen zu steuern und zu beeinflussen.
Paternòs Arbeit ging jedoch über die akademische Welt hinaus und hatte tiefgreifende Auswirkungen auf die moderne Chemie und, in der Folge, auch auf die pharmazeutische Industrie. Die Möglichkeit, durch photochemische Reaktionen Oxetan-Ringe zu erzeugen, brachte neue Ansätze im Bereich des Wirkstoffdesigns und der Arzneimittelentwicklung hervor. Diese viergliedrigen Ringe besitzen einzigartige chemische Eigenschaften, die die Aktivität und Stabilität von pharmazeutischen Wirkstoffen verbessern können. Heute werden Oxetan-haltige Moleküle intensiv erforscht, da sie in der Lage sind, biologische Ziele mit hoher Spezifität zu beeinflussen, was die Wirksamkeit von Therapien in Bereichen wie Onkologie und Antibiotikaforschung steigern kann. Dieser Ansatz, der in Paternòs Entdeckung wurzelt, zeigt die weitreichenden Auswirkungen seiner Forschung und ihren wichtigen Beitrag zur modernen medizinischen Chemie.
Im Laufe seiner Karriere engagierte sich Paternò auch intensiv in der Lehre und in der wissenschaftlichen Kommunikation. Er betreute und prägte eine Generation von Chemikern, die das Fachgebiet weiter voranbrachten und seine Prinzipien der genauen Experimentation und forschungsgetriebenen Neugier weitertrugen. Sein Vermächtnis beschränkt sich nicht nur auf seine eigenen Entdeckungen, sondern spiegelt sich auch in der Arbeit unzähliger Wissenschaftler wider, die auf seinen Ideen und Techniken aufbauen konnten. Durch die Brücke, die er zwischen Photochemie und organischer Synthese schlug, hinterließ Emanuele Paternò einen unauslöschlichen Eindruck in der Wissenschaftslandschaft. Seine Beiträge inspirieren künftige Generationen und fördern den kontinuierlichen Fortschritt der Chemie und Pharmazie. Seine Arbeit ist ein Zeugnis für die Kraft der Innovation, der Neugier und der tiefgreifenden Wirkung der Grundlagenforschung.
Mario Passerini war ein bahnbrechender italienischer Chemiker, dessen Beiträge zur organischen Chemie bis heute wissenschaftliche Fortschritte prägen. Seine bedeutendste Errungenschaft, die Passerini-Reaktion, ist nach wie vor ein Eckpfeiler in der Synthese komplexer Moleküle. Geboren im frühen 20. Jahrhundert, widmete Passerini seine akademische Laufbahn der Erforschung von Mehrkomponentenreaktionen, was zur Entdeckung seiner gleichnamigen Reaktion führte. Diese Transformation, die die effiziente Bildung von α-Hydroxycarbonsäureamiden aus Carbonylverbindungen, Isocyaniden und Carbonsäuren ermöglicht, revolutionierte die organische Synthese, indem sie die Konstruktion strukturell vielseitiger Verbindungen in einem einzigen Schritt erlaubt.
Die Passerini-Reaktion hat die pharmazeutische Industrie nachhaltig beeinflusst, da sie einen effizienten Weg zur Entwicklung biologisch aktiver Moleküle bietet. Ihre Fähigkeit, molekulare Komplexität mit hoher Atomeffizienz zu erzeugen, macht sie zu einem wertvollen Werkzeug in der Wirkstoffforschung und medizinischen Chemie. Viele moderne Arzneimittel nutzen Mehrkomponentenreaktionen, die von Passerinis Arbeiten inspiriert wurden, um schnell umfangreiche Wirkstoffbibliotheken für die Identifikation neuer Therapeutika zu synthetisieren. Seine Forschung legte das Fundament für Fortschritte sowohl in der Naturstoffsynthese als auch in der Polymerchemie und beeinflusste die Entwicklung funktionalisierter Materialien für medizinische Anwendungen.
ChemCon ist ein zukunftsorientierter Akteur im Bereich der medizinischen Chemie und GMP-Polymere und baut auf den Grundlagen auf, die Pioniere wie Passerini geschaffen haben. Das Unternehmen ist auf kundenspezifische Synthesen spezialisiert und entwickelt hochreine Verbindungen, die strenge regulatorische Anforderungen erfüllen. Da sich die pharmazeutische Forschung stetig weiterentwickelt, ist die präzise und konsistente Herstellung spezialisierter Moleküle von entscheidender Bedeutung. ChemCons Expertise in GMP-Polymeren stellt sicher, dass innovative Materialien für fortschrittliche medizinische Anwendungen, von Wirkstofffreisetzungssystemen bis hin zu biokompatiblen Beschichtungen, verfügbar sind. Mit einem starken Fokus auf Qualität und Innovation schlägt ChemCon die Brücke zwischen bahnbrechender Forschung und realen Anwendungen und zeigt, wie relevant Passerinis Arbeit in der heutigen pharmazeutischen und Materialwissenschaft ist.
Peter L. Pauson, eine prominente Persönlichkeit in der Welt der Chemie, leistete bedeutende Beiträge auf dem Gebiet der metallorganischen Chemie. Geboren am 23. August 1925 in Berlin, Deutschland, wuchs Pauson in einer Zeit erheblicher globaler Veränderungen auf und zog schließlich nach Großbritannien. Er absolvierte sein Studium am University College London, wo er eine starke Grundlage in Chemie erwarb, die später seine Karriere prägen sollte.
Pausons bemerkenswerteste Errungenschaft ist die Entwicklung der Pauson-Khand-Reaktion, eine Zusammenarbeit mit Ihsan Khand. Diese Reaktion ist aufgrund ihrer Effizienz und Vielseitigkeit zu einem Eckpfeiler der synthetischen organischen Chemie geworden. Die Pauson-Khand-Reaktion ist ein 2+2+1-Cycloadditionsprozess, der die Wechselwirkung eines Alkens, eines Alkyns und Kohlenmonoxids beinhaltet, wobei Dicobaltoctacarbonyl als Katalysator verwendet wird. Diese Reaktion führt zur Bildung substituierter Cyclopentenone, die für die Synthese komplexer organischer Moleküle unerlässlich sind. Die Fähigkeit, fünfgliedrige Ringe zu konstruieren, die in Naturprodukten und Pharmazeutika häufig vorkommen, hat diese Reaktion zu einem unverzichtbaren Werkzeug für Chemiker gemacht.
Der Einfluss von Pausons Arbeit reicht weit über die Pauson-Khand-Reaktion hinaus. Seine Pionierarbeit in der metallorganischen Chemie hat den Weg für weitere Innovationen in der Synthese komplexer Moleküle und der Untersuchung von Metall-Organischen Gerüsten geebnet. Seine Forschung hat die Entwicklung neuer katalytischer Prozesse beeinflusst und das Verständnis chemischer Reaktionen und Mechanismen vorangetrieben.
Peter Pausons Vermächtnis in der Chemie ist geprägt von seiner Hingabe an das Fachgebiet und seinen Beiträgen zur Weiterentwicklung der modernen Chemie. Seine Arbeit inspiriert und beeinflusst Chemiker weltweit und spiegelt den tiefgreifenden Einfluss wider, den er auf die wissenschaftliche Gemeinschaft hatte.
Hans von Pechmann, geboren am 1. April 1850 in Mülhausen, Elsass, war eine bahnbrechende Persönlichkeit auf dem Gebiet der organischen Chemie. Sein Weg in die Wissenschaft begann mit seinem Studium an der Universität München unter der Mentorschaft von Adolf von Baeyer, wo er ein tiefes Interesse an der Synthese organischer Verbindungen entwickelte.
Die Beiträge Pechmanns zur Chemie sind zahlreich, wobei seine Entwicklung der Pechmann-Kondensationsreaktion zu den bemerkenswertesten gehört. Diese Reaktion, die Coumarine aus Phenolen und β-Ketoestern in Gegenwart von Säuren synthetisiert, hat neue Wege in der Synthese von Naturprodukten und heterozyklischen Verbindungen eröffnet, die für Pharmazeutika und Farbstoffe von entscheidender Bedeutung sind.
Ein weiterer bedeutender Erfolg Pechmanns war die Entdeckung von Polyethylen im Jahr 1898, ein Ergebnis seiner Experimente mit Diazomethan. Diese Entdeckung legte den Grundstein für die Entwicklung von Kunststoffen und revolutionierte Industrien von der Verpackung bis zur Telekommunikation. Heutzutage werden Polymere umfangreich für pharmazeutische Anwendungen genutzt, einschließlich der Herstellung von Medikamenten, wobei Good Manufacturing Practice (GMP) Polymere als Hilfsstoffe dienen, die die Stabilität, Wirksamkeit und Abgabe von Wirkstoffen verbessern. Ihre Haltbarkeit und Flexibilität haben Polymere unverzichtbar in der modernen Welt gemacht.
Pechmanns Arbeit trug nicht nur zum Fortschritt der chemischen Synthese und Polymerwissenschaft bei; sie inspirierte auch zukünftige Generationen von Chemikern. Trotz seines Todes am 19. April 1902 lebt sein Erbe durch die Pechmann-Reaktion und die weitverbreitete Nutzung von Polymeren weiter und unterstreicht die Auswirkungen seiner Innovationen auf das moderne Leben und das Feld der Chemie.
Sir William Henry Perkin, geboren am 12. März 1838 in London, war ein renommierter Chemiker, dessen zufällige Entdeckung die Textilindustrie revolutionierte und die Welt der Wissenschaft unauslöschlich geprägt hat.
Perkins Weg in die Chemie begann schon in jungen Jahren, als er ein reges Interesse an der Wissenschaft zeigte. Er setzte seine akademischen Bemühungen am Royal College of Chemistry unter der Mentorschaft von August Wilhelm von Hofmann, einem bedeutenden Chemiker seiner Zeit, fort.
Bei dem Versuch, Chinin, ein Medikament zur Behandlung von Malaria, zu synthetisieren, stieß Perkin 1856 auf einen unerwarteten Durchbruch. Anstelle von Chinin entdeckte er einen leuchtend violetten Farbstoff, den er später "Mauveine" oder "Mauve" nannte. Diese zufällige Kreation erwies sich als bahnbrechend für die Textilindustrie, da sie eine kostengünstige Alternative zu natürlichen Farbstoffen darstellte und eine Revolution im Bereich der Farben auslöste.
Perkin erkannte das kommerzielle Potenzial seiner Entdeckung und gründete eine chemische Produktionsfirma, um synthetische Farbstoffe in industriellem Maßstab herzustellen. Sein Unternehmergeist und seine wissenschaftlichen Fähigkeiten verhalfen ihm zu großem Erfolg und machten ihn zu einer führenden Persönlichkeit in der chemischen Industrie.
Perkins Beiträge gingen über die Entdeckung des Mauveins hinaus. Er setzte seine Innovationstätigkeit fort und führte eine Reihe synthetischer Farbstoffe ein, die die Modeindustrie veränderten und in der Druckerei und Fotografie Anwendung fanden.
Neben seinen Leistungen in der Industrie waren Perkins akademische Aktivitäten ebenso bemerkenswert. Seine Studien am Royal College of Chemistry legten den Grundstein für seine bahnbrechenden Forschungen, und seine Betreuung durch Hofmann förderte seine Leidenschaft für die Chemie.
Perkins Vermächtnis ist ein Zeugnis für die Kraft der wissenschaftlichen Neugier und Innovation. Seine zufällige Entdeckung des Mauveins revolutionierte nicht nur die Textilindustrie, sondern veränderte auch die Art und Weise, wie wir Farbe und Kreativität wahrnehmen.
Sir William Henry Perkin, der 1906 für seine Beiträge zur Chemie zum Ritter geschlagen wurde, ist nach wie vor eine gefeierte Persönlichkeit in der wissenschaftlichen Gemeinschaft, und sein Name ist ein Synonym für Fortschritt und Einfallsreichtum im Bereich der Chemie.
Amé Pictet, geboren 1857 in Genf, war ein herausragender Schweizer Chemiker, dessen Arbeiten die organische Chemie und die pharmazeutische Wissenschaft maßgeblich beeinflussten. Nach seinem Studium an der Universität Genf widmete sich Pictet intensiv der Erforschung der heterocyclischen Chemie und schuf dadurch Erkenntnisse, die die Grundlagen vieler späterer Entwicklungen in der Pharmakologie legten. Schon früh in seiner Karriere zeichnete er sich durch sein Streben aus, komplexe organische Moleküle zu verstehen, und seine Forschungsergebnisse haben bis heute einen prägenden Einfluss.
Einer seiner bemerkenswerten Beiträge ist die Pictet-Gams-Synthese, die er zusammen mit dem österreichischen Chemiker Theodor Gams entwickelte. Diese Reaktion gehört zu einer Reihe von Prozessen, die seinen Namen tragen, darunter die Pictet-Spengler-Reaktion. Die Pictet-Gams-Synthese konzentriert sich auf die Bildung von Isochinolin-Derivaten, die eine Grundlage für die Herstellung zahlreicher Verbindungen mit verschiedenen medizinischen Anwendungen bilden. Isochinoline sind stickstoffhaltige Heterozyklen und dienen als Grundgerüst für viele natürliche und synthetische Alkaloide, von denen einige in der Schmerztherapie, in der Malariabehandlung und sogar in der Onkologie eingesetzt werden. Die Vielseitigkeit von Isochinolinen, auf biologische Mechanismen einzuwirken, macht sie in der modernen Arzneimittelentwicklung unverzichtbar. Sie erlauben es Forschern, ihre Wirkungen gezielt an spezifische zelluläre Prozesse anzupassen, um effektivere Therapieansätze zu entwickeln.
Die Pictet-Gams-Synthese ermöglicht die Bildung solcher Verbindungen mit einer damals bahnbrechenden Effizienz und Präzision. Durch die Kombination eines Arylamins mit einem Aldehyd oder Keton und eine anschließende säurekatalysierte Cyclisierung lassen sich diese komplexen Strukturen in wenigen Schritten und mit hoher Reinheit erzeugen. Diese Methode stellte nicht nur einen bedeutenden Fortschritt für die synthetische Chemie dar, sondern bot auch der pharmazeutischen Industrie eine verlässliche Grundlage zur Herstellung von Arzneimitteln auf Isochinolinbasis. Isochinolin-Derivate werden zur Entwicklung einer breiten Palette an Medikamenten verwendet, von Analgetika wie Morphin bis hin zu Antitussiva und bestimmten Krebsmedikamenten.
Für seine herausragenden Leistungen in der Chemie wurde Pictet in akademischen und beruflichen Kreisen hoch geschätzt und mit verschiedenen Ehrungen und Preisen ausgezeichnet. Er veröffentlichte zahlreiche Arbeiten, die für ihre methodische Strenge und ihren innovativen Ansatz anerkannt wurden. Der Einfluss von Pictets Arbeiten auf die medizinische Chemie ist kaum zu überschätzen; die von ihm entwickelten Werkzeuge und Techniken prägen bis heute die Synthese komplexer organischer Verbindungen, die essenziell für die moderne Arzneimittelentwicklung sind.
Durch die Pictet-Gams-Synthese und seine bahnbrechenden Forschungen zu Isochinolin-Derivaten legte Amé Pictet das Fundament für die moderne medizinische Chemie. Sein Erbe lebt weltweit in Laboratorien und pharmazeutischen Unternehmen weiter, wo seine Methoden die Entwicklung neuer, wirksamer Medikamente ermöglichen, die sich einigen der drängendsten Gesundheitsprobleme unserer Zeit widmen.
Paul Fritsch, ein bedeutender Chemiker des frühen 20. Jahrhunderts, prägte die organische Chemie nachhaltig, insbesondere durch die Entwicklung der Pomeranz-Fritsch-Reaktion. Geboren im 19. Jahrhundert, widmete sich Fritsch dem Studium und der Synthese komplexer Moleküle, wobei er sich besonders auf Heterocyclen konzentrierte. Diese Arbeit war von grundlegender Bedeutung sowohl für die theoretische Chemie als auch für praktische Anwendungen, die bis heute Bestand haben.
Fritsch durchlief seine akademische Ausbildung in einer Zeit intensiver chemischer Entdeckungen und konnte sich durch seine außergewöhnlichen Forschungsergebnisse bald einen Namen machen. Während seiner Karriere als Forscher und Lehrer publizierte er zahlreiche Arbeiten, die das Wissen über chemische Synthese vorantrieben. Obwohl er im Vergleich zu anderen bekannten Chemikern seiner Zeit vielleicht weniger Anerkennung erhielt, ist sein Einfluss auf die Wissenschaft deutlich spürbar. Ein Höhepunkt seines Schaffens war die gemeinsame Entwicklung der Pomeranz-Fritsch-Reaktion mit Karl Pomeranz, die eine einfache Methode zur Synthese von Isochinolin-Derivaten darstellt – einer Molekülklasse, die in der pharmazeutischen Forschung von großer Bedeutung ist.
Die Pomeranz-Fritsch-Reaktion ermöglicht die Synthese von Isochinolinen durch eine elegante Cyclisierungsreaktion, bei der Benzaldehyd und ein 2,2-Dialkoxyethylamin miteinander reagieren. Diese Reaktion führt zu einem Isochinolin-Derivat. Sie ist besonders vielseitig, da sie nicht auf ein spezielles Diethylacetal beschränkt ist, sondern auch mit anderen 2,2-Dialkoxyethylaminen durchgeführt werden kann. Durch diese Methode können Isochinolin-Derivate relativ effizient hergestellt werden. Dies war ein Meilenstein, da die Reaktion einen einfachen Zugang zu komplexen heterocyclischen Strukturen eröffnet und somit eine zentrale Grundlage für die Entwicklung von Arzneimitteln schafft. Isochinoline und ihre Derivate sind aromatische Heterocyclen, die in der pharmazeutischen Chemie sehr geschätzt werden – insbesondere aufgrund ihrer Vielseitigkeit und biologischen Aktivität. Sie dienen oft als Gerüststruktur in vielen Wirkstoffen und spielen eine entscheidende Rolle in der Entwicklung von Medikamenten.
Die Bedeutung der Isochinolin-Derivate für die Pharmaindustrie ist enorm. Viele Medikamente, die gegen Malaria, Bluthochdruck oder sogar Krebs eingesetzt werden, basieren auf Isochinolin-Strukturen. Dank ihrer Fähigkeit, mit unterschiedlichen biologischen Zielstrukturen zu interagieren, sind Isochinoline unverzichtbar für die Entwicklung neuer Wirkstoffe. So finden sich Isochinolin-Bausteine in pharmazeutischen Wirkstoffen, die unter anderem zur Behandlung von Schmerzen, Infektionen, Herz-Kreislauf-Erkrankungen und neurologischen Störungen eingesetzt werden.
Die Pomeranz-Fritsch-Reaktion erleichtert dabei nicht nur die Herstellung, sondern ermöglicht es Chemikern, strukturelle Modifikationen an den Isochinolin-Bausteinen vorzunehmen und neue, wirksamere und verträglichere Substanzen zu entwickeln. Damit ebnete die Reaktion den Weg für zahllose Innovationen in der organischen Synthese und schuf die Grundlage für die Entdeckung vieler neuer therapeutischer Verbindungen. Auch heute noch inspirieren die Erkenntnisse aus Fritschs Arbeit Chemiker weltweit, auf Basis dieser Reaktion weiterzuforschen und neue Lösungen für gesundheitliche Herausforderungen zu entwickeln.
Paul Fritschs Vermächtnis zeigt sich in der bleibenden Relevanz der von ihm mitentwickelten Reaktion und der durch sie ermöglichten Fortschritte in der modernen Arzneimittelentwicklung. Isochinolin-Derivate sind heute eine unverzichtbare Komponente der medizinischen Chemie, und die Pomeranz-Fritsch-Reaktion bleibt ein fundamentales Werkzeug im Arsenal der organischen Synthese. In den Händen heutiger Wissenschaftler setzt Fritschs Arbeit ihren Weg fort und trägt dazu bei, therapeutische Innovationen für eine bessere Gesundheit der Menschen zu ermöglichen.
Robert Pschorr, geboren am 13. März 1868 in München, Deutschland, war ein herausragender Chemiker, dessen Beitrag zur organischen Chemie nachhaltig wirkt. Er studierte an der Universität München, wo er von dem renommierten Chemiker Adolf von Baeyer, einem Nobelpreisträger, betreut wurde.
Pschorrs Arbeit konzentrierte sich hauptsächlich auf die Synthese und strukturelle Analyse komplexer organischer Moleküle. Er machte bedeutende Fortschritte im Bereich aromatischer Verbindungen, die entscheidend für die Entwicklung von Farbstoffen, Arzneimitteln und vielen anderen chemischen Produkten sind.
Unter seinen zahlreichen Beiträgen ragt die Pschorr-Cyclisierung als bahnbrechende Leistung heraus. Diese Reaktion ist ein intramolekularer Substitutionsprozess, der Aryldiazoniumsalze involviert. In Gegenwart eines Kupferkatalysators und salpetriger Säure durchlaufen diese Salze eine Cyclisierungsreaktion zur Bildung polycyclischer aromatischer Verbindungen. Diese Methode war entscheidend für die Synthese verschiedener komplexer Moleküle in der organischen Chemie, insbesondere in der pharmazeutischen Industrie.
Pschorrs Einfluss erstreckte sich über seine eigene Forschung hinaus. Ein weiterer bedeutender Mentor auf seinem akademischen Weg war Ludwig Knorr, ein renommierter Chemiker, der für seine wegweisenden Arbeiten in der heterocyclischen Chemie bekannt ist. Knorrs Mentorschaft beeinflusste Pschorrs Ansatz zur organischen Synthese und prägte sein innovatives Denken auf diesem Gebiet.
Robert Pschorrs innovative Ansätze und seine Mentorschaft unter Chemikern wie Ludwig Knorr und Adolf von Baeyer haben bleibende Spuren in der organischen Chemie hinterlassen. Seine bahnbrechende Arbeit zur Pschorr-Cyclisierung bleibt ein wichtiges Werkzeug für Chemiker weltweit und zeigt die anhaltende Bedeutung seiner wissenschaftlichen Beiträge.
Bronisław Leonard Radziszewski wurde 1838 in Warschau geboren. 1855 beendete er das Gymnasium in Warschau und begann daraufhin ein Studium der Naturwissenschaften in Moskau. Nach seinem Studium war er im Jahr 1862 Naturkundelehrer am III. Gymnasium in Warschau. Er war aktiv am Januaraufstand im Jahr 1863 beteiligt. Nach dem Scheitern des Aufstands verließ er Polen, um zwischen 1864 und 1867 in Gent unter August Kekulé Chemie zu studieren. Er promovierte 1867 und war danach bis 1870 Chemie-Assistent an der Universität Leuven. Nach seiner Zeit in Belgien kehrte er nach Polen zurück und wurde stellvertretender Professor für Chemie am Technischen Institut in Krakau. Zusätzlich war er Lehrer an der Realschule. 1872 wurde er Professor für allgemeine und pharmazeutische Chemie in Lwów und somit der erste auf Polnisch lehrende Chemieprofessor dort. Er leitete auch den Lehrstuhl für Pharmazie und war Direktor des Chemischen Instituts. 1874 war er Mitbegründer der Polnischen Gesellschaft der Naturwissenschaftler Kopernikus. Ab 1879 war Radziszewski Dekan der Philosophischen Fakultät und ab 1882 Rektor der Universität Lwów.
Die Radziszewski-Synthese wird dazu verwendet, um Imidazole darzustellen. Imidazol ist ein Strukturelement des Hormons Histamin. Heutzutage kann Histamin durch Decarboxylierung der Aminosäure Histidin auch synthetisch hergestellt werden. Histamin wird unter anderem in einem Medikament zur Behandlung seltener Formen von Leukämie und in Allergietests verwendet. Damit Histamin in Medikamenten verwendet werden darf, muss es unter strengen GMP-Bedingungen produziert werden.
Das Leben und Vermächtnis von Leopold Ružička: Pionierarbeit an den Grenzen der Chemie
In den Annalen wissenschaftlicher Errungenschaften gibt es nur wenige, die so tiefgreifende Spuren hinterlassen haben wie Leopold Ružička, ein Visionär, dessen Arbeit nicht nur die Chemie voranbrachte, sondern auch den Grundstein für zahllose Innovationen in der Medizin, der Parfümerie und darüber hinaus legte. Geboren am 13. September 1887 in Vukovar, damals Teil der Österreichisch-Ungarischen Monarchie (heute Kroatien), ist Ružičkas Weg von einer Kleinstadt an die Spitze wissenschaftlicher Anerkennung ein Zeugnis für die anhaltende Kraft von Neugierde und Beharrlichkeit.
Frühes Leben und Ausbildung
Ružičkas akademischer Weg begann an der Technischen Universität Karlsruhe, wo er Chemieingenieurwesen studierte. Sein Wechsel an die Universität Zürich, wo er unter der Leitung von Professor Hermann Staudinger promovierte, legte jedoch den Grundstein für seine bahnbrechenden Arbeiten. Staudinger, selbst Nobelpreisträger, weckte in Ružička die Leidenschaft für die organische Chemie, insbesondere für das Studium der Naturstoffe.
Akademische Errungenschaften und Forschung
Ružičkas Karriere zeichnete sich durch seine bahnbrechenden Forschungen auf dem Gebiet der Chemie der Naturstoffe aus. Seine frühen Arbeiten befassten sich mit der Untersuchung von Terpenen, einer Klasse organischer Verbindungen, die in ätherischen Ölen und Pflanzenharzen vorkommen und für die Duft- und Aromenindustrie von entscheidender Bedeutung sind. Ružičkas Untersuchungen zur Struktur und Synthese von Terpenen legten den Grundstein für die moderne organische Synthese, die es Chemikern ermöglicht, komplexe organische Moleküle im Labor herzustellen.
Der vielleicht bedeutendste Beitrag von Ružička war seine Forschung zu den Geschlechtshormonen. In den 1930er Jahren synthetisierte er mehrere wichtige Hormone, darunter Testosteron und Androsteron, und revolutionierte damit das Studium der Biochemie und Endokrinologie. Seine Arbeit trug nicht nur zum besseren Verständnis der menschlichen Biologie bei, sondern hatte auch praktische Anwendungen in der Medizin, etwa bei der Behandlung von Hormonstörungen und der Entwicklung von Verhütungsmitteln.
Nobelpreis und Einfluss auf die moderne Chemie
In Anerkennung seiner Beiträge zur Erforschung organischer Verbindungen wurde Ružička 1939 mit dem Nobelpreis für Chemie "für seine Arbeiten über Polymethylene und höhere Terpene" ausgezeichnet. Diese Auszeichnung war die Krönung jahrelanger akribischer Forschung und Innovation und unterstreicht seine Rolle bei der Erweiterung der Grenzen der organischen Chemie.
Ružičkas Einfluss auf die moderne Chemie geht über seine mit dem Nobelpreis ausgezeichnete Arbeit hinaus. Er war ein Pionier des Konzepts der chemischen Synthese und zeigte, dass es möglich ist, komplexe natürliche Moleküle im Labor nachzubauen und zu verändern. Dieses Prinzip ist zu einem Eckpfeiler der modernen pharmazeutischen Chemie geworden, in der die Synthese eine entscheidende Rolle bei der Arzneimittelentwicklung spielt.
Erbe und Wirkung
Neben seinen wissenschaftlichen Leistungen war Ružička auch ein Mentor für künftige Generationen von Chemikern. Als Professor an der Eidgenössischen Technischen Hochschule in Zürich inspirierte er unzählige Studenten mit seinem Engagement für Forschung und Innovation. Sein Vermächtnis besteht nicht nur in den Molekülen, die er entdeckte oder synthetisierte, sondern auch in den Köpfen, die er formte, und in der wissenschaftlichen Gemeinschaft, die er förderte.
Leopold Ružičkas Beiträge zur Chemie waren wegweisend. Indem er die Komplexität organischer Moleküle entschlüsselte, brachte er nicht nur das Fachgebiet der Chemie voran, sondern hatte auch tiefgreifende Auswirkungen auf Medizin, Industrie und Landwirtschaft. Seine Arbeit ist ein Beispiel für die Kraft der Wissenschaft, die Geheimnisse der natürlichen Welt zu entschlüsseln und das Leben der Menschen zu verbessern. Während wir weiterhin die Grenzen der Wissenschaft erforschen, bleibt Ružičkas Pioniergeist ein wegweisendes Licht, das uns an die unendlichen Möglichkeiten erinnert, die uns auf der Suche nach Wissen erwarten.
Roland Scholl, ein Name, der eng mit einem entscheidenden Fortschritt in der organischen Chemie verbunden ist, war ein herausragender Chemiker, dessen Beiträge das Fachgebiet nachhaltig geprägt haben. Scholls Weg in die Chemie war von unerschütterlicher Neugier und einem tiefen Engagement für wissenschaftliche Entdeckungen geprägt. Seine akademische Laufbahn war durch eine Reihe bahnbrechender Errungenschaften gekennzeichnet, die die moderne organische Chemie erheblich beeinflussten.
Scholls bekanntester Beitrag ist die Scholl-Reaktion, eine Kupplungsreaktion, die zu den Grundpfeilern der Synthese aromatischer Verbindungen gehört. Diese Reaktion, die er in der Mitte des 20. Jahrhunderts entwickelte, erfolgt in Gegenwart katalytischer Mengen von Lewis-Säuren und ermöglicht die Kopplung aromatischer Verbindungen. Die Scholl-Reaktion wird für ihre Fähigkeit geschätzt, komplexe aromatische Systeme aus einfacheren Ausgangsmaterialien zu erzeugen, was sie zu einem wertvollen Werkzeug in Forschung und Industrie macht.
Der Mechanismus der Scholl-Reaktion ist sowohl elegant als auch effizient. Durch die Nutzung der einzigartigen Reaktivität von Lewis-Säuren erlaubt Scholls Methode die Bildung von Kohlenstoff-Kohlenstoff-Bindungen zwischen aromatischen Ringen, was zur Schaffung neuer, strukturell vielfältiger aromatischer Verbindungen führt. Dieser Ansatz hat sich als entscheidend bei der Entwicklung verschiedener chemischer Produkte erwiesen, darunter Farbstoffe, Arzneimittel und fortschrittliche Materialien.
Scholls Arbeit war nicht nur in ihrem chemischen Ansatz innovativ, sondern auch maßgeblich für das Verständnis der Aromatenchemie. Seine Forschung lieferte neue Einblicke in das Verhalten aromatischer Systeme, was weitreichende Implikationen für die theoretische und angewandte Chemie hatte. Die Scholl-Reaktion veranschaulicht, wie grundlegende wissenschaftliche Forschung zu praktischen Anwendungen führen kann, die Industrie und technologische Fortschritte vorantreiben.
Das Erbe von Roland Scholl reicht über seine individuellen Errungenschaften hinaus. Seine Arbeit ebnete den Weg für weitere Entwicklungen in der chemischen Synthese und inspirierte unzählige Chemiker, seine Entdeckungen zu erforschen und weiterzuentwickeln. Die Prinzipien, die der Scholl-Reaktion zugrunde liegen, sind auch in der zeitgenössischen Forschung von Bedeutung, und die Reaktion selbst bleibt ein unverzichtbares Werkzeug in der organischen Chemie.
Im weiteren Kontext der chemischen Industrie haben Scholls Beiträge Fortschritte in der Produktion einer Vielzahl von chemischen Produkten ermöglicht. Die Fähigkeit, komplexe aromatische Verbindungen effizient zu synthetisieren, hat die Entwicklung neuer Materialien und Technologien gefördert, die verschiedene Branchen beeinflussen, von der Pharmaindustrie bis zur Materialwissenschaft.
Das Erbe von Roland Scholl ist ein Beweis für den tiefgreifenden Einfluss, den ein engagierter Wissenschaftler auf sein Fachgebiet und die Welt im Allgemeinen haben kann. Sein innovativer Ansatz zur Chemie hat nicht nur unser Verständnis der aromatischen Verbindungen bereichert, sondern auch praktische Werkzeuge bereitgestellt, die weiterhin den Fortschritt in der chemischen Industrie vorantreiben. Wenn wir auf seine Beiträge zurückblicken, werden wir an den anhaltenden Einfluss seiner Arbeit und die fortwährende Relevanz seiner Entdeckungen für die Zukunft der Chemie erinnert.
Sharpless studierte am Darthmouth College. Im Jahr 1968 promovierte er in organischer Chemie an der Stanford University.
Zusammen mit William S. Knowles und Ryoji Noyori erhielt Sharpless 2001 den Nobelpreis für Chemie für Arbeiten auf dem Gebiet stereoselektive Oxidationsreaktionen und 2022 erhielt er zusammen mit Carolyn Bertozzi und Morten Meldal seinen zweiten Nobelpreis für Chemie (für grundlegende Arbeiten in der Click-Chemie). Somit ist er neben Frederick Sanger die einzige Person, die zweimal mit dem Nobelpreis für Chemie ausgezeichnet wurde.
Kenkichi Sonogashira war ein japanischer Chemiker, dessen bahnbrechende Arbeit die organische Chemie nachhaltig beeinflusst hat. Er wurde 1931 in Kyoto geboren und zeigte schon früh eine bemerkenswerte Begabung für Naturwissenschaften. Nach seinem Studium der Chemie an der Universität Kyoto widmete er sich der organischen Synthese, einem Bereich, der zu seiner Zeit enorme Fortschritte machte. Sonogashira verfolgte das Ziel, Reaktionen zu entwickeln, die effizienter, umweltfreundlicher und vielseitiger einsetzbar sind. In den 1970er Jahren gelang ihm eine Entdeckung, die seinen Namen weltweit bekannt machen sollte: die nach ihm benannte Sonogashira-Kupplung.
Diese Reaktion, eine Kreuzkupplung zwischen Aryl- oder Vinylhalogeniden und terminalen Alkinen, eröffnete neue Möglichkeiten in der Synthese organischer Moleküle. Die Reaktion nutzt einen Palladiumkatalysator in Kombination mit einem Kupfer(I)-Ko-Katalysator und ist bemerkenswert für ihre Effizienz und ihre Fähigkeit, unter milden Bedingungen abzulaufen. Besonders revolutionär war die Tatsache, dass sie es ermöglichte, C-C-Dreifachbindungen auf einfache Weise zu etablieren, was zuvor ein großes Problem in der organischen Synthese darstellte. Die Sonogashira-Kupplung fand schnell Anwendung in der Herstellung komplexer Moleküle, darunter Naturstoffe, funktionelle Materialien und pharmazeutische Wirkstoffe.
In der modernen Forschung wurde die Sonogashira-Kupplung weiter optimiert. Wissenschaftler haben Varianten entwickelt, die ohne Kupfer auskommen, um die Bildung unerwünschter Nebenprodukte wie Homokupplungen zu minimieren. Zudem wurden umweltfreundlichere Katalysatorsysteme untersucht, die kostengünstiger und weniger toxisch sind. Neueste Studien haben gezeigt, dass die Reaktion auch in wässrigen Medien oder unter mikrowellenunterstützten Bedingungen durchgeführt werden kann, was ihre Nachhaltigkeit weiter verbessert. Darüber hinaus wird intensiv daran gearbeitet, diese Kupplung in industriellen Prozessen effizienter zu machen, beispielsweise durch den Einsatz kontinuierlicher Durchflussreaktoren.
Die Bedeutung der Sonogashira-Kupplung für die pharmazeutische Industrie kann kaum überschätzt werden. Viele Arzneimittel enthalten Struktureinheiten, die durch diese Reaktion zugänglich gemacht werden können, wie etwa Alkine oder konjugierte Systeme. Sie wird regelmäßig bei der Synthese von Krebsmedikamenten, antiviralen Wirkstoffen und Diagnostikmitteln eingesetzt. Auch in der Materialwissenschaft ist die Reaktion unverzichtbar, insbesondere bei der Herstellung organischer Leuchtdioden (OLEDs) und leitfähiger Polymere, die für moderne Elektronik entscheidend sind.
Kenkichi Sonogashira hat mit seiner Reaktion eine Grundlage geschaffen, die weit über seine ursprüngliche Entdeckung hinausgeht. Sein Vermächtnis zeigt, wie eine einzelne chemische Transformation die Art und Weise verändern kann, wie wir Moleküle entwickeln und einsetzen. Bis heute inspiriert seine Arbeit Chemiker weltweit, neue Wege in der organischen Synthese zu erkunden und die Grenzen des Möglichen zu erweitern.
Hermann Staudinger, ein bahnbrechender deutscher Chemiker und Nobelpreisträger, hinterließ durch seine wegweisende Arbeit an Makromolekülen und die Entwicklung der Staudinger-Reaktion einen unauslöschlichen Eindruck in der Chemie. Geboren am 23. März 1881 in Worms, begann Staudinger seine akademische Laufbahn mit dem Chemiestudium an den Universitäten Halle, Darmstadt und München. Nach seiner Promotion im Jahr 1903 unter der Anleitung von Daniel Vorländer schlug Staudinger einen Weg ein, der letztlich unser Verständnis von großen Molekülen, heute bekannt als Polymere, revolutionieren sollte.
Staudingers frühe akademische Erfolge waren bemerkenswert, auch wenn sie zunächst nicht auf den revolutionären Weg hinwiesen, den er später einschlagen würde. Zu Beginn konzentrierte er sich auf die organische Chemie und trug wesentlich zum Verständnis von Ketenen und deren Reaktivität bei. Diese Arbeit legte den Grundstein für seine späteren Entdeckungen und zeigte bereits seine Fähigkeit, unerforschte Gebiete der Chemie zu erkunden. Im Jahr 1919 entdeckte Staudinger während seiner Tätigkeit an der Technischen Hochschule Karlsruhe die nach ihm benannte Staudinger-Reaktion, eine Methode zur Synthese von primären Aminen aus Aziden. Diese Reaktion, die die Reduktion von Aziden durch Triphenylphosphan zur Bildung eines Iminophosphoran-Zwischenprodukts umfasst, war ein bedeutender Fortschritt in der organischen Synthese und demonstrierte Staudingers innovativen Ansatz bei chemischen Reaktionen.
Doch es war Staudingers Arbeit an Makromolekülen, die ihn wirklich auszeichnete. Anfang der 1920er Jahre, als Professor an der Universität Zürich, begann Staudinger, die damals vorherrschende Vorstellung zu hinterfragen, dass Polymere lediglich Aggregate kleiner Moleküle seien, die durch schwache zwischenmolekulare Kräfte zusammengehalten werden. Er schlug stattdessen vor, dass Polymere lange Ketten aus kovalent gebundenen Atomen seien – ein Konzept, das zunächst auf Skepsis stieß. Staudingers Beharrlichkeit und sein unermüdliches Bestreben, seine Theorie zu beweisen, führten schließlich zur Anerkennung des makromolekularen Konzepts und veränderten grundlegend das Verständnis von Materialien wie Gummi, Kunststoffen und Fasern.
Im Jahr 1926 nahm Staudinger eine Professur an der Universität Freiburg im Breisgau an, wo er den Rest seiner Karriere verbringen sollte. Seine Zeit in Freiburg war geprägt von intensiver Forschung und zahlreichen Veröffentlichungen, die seinen Ruf als führender Chemiker weiter festigten. In dieser Phase leistete Staudinger seine bedeutendsten Beiträge zur Polymerforschung. Er und seine Mitarbeiter führten Experimente durch, die das hohe Molekulargewicht dieser Substanzen nachwiesen und damit die empirischen Belege lieferten, die zur Unterstützung seiner makromolekularen Theorie notwendig waren. Diese Arbeit legte den Grundstein für die Entwicklung der Polymerchemie als eigenständiges Forschungsgebiet und hatte weitreichende Auswirkungen auf Industrien von der Textil- bis zur Pharmaindustrie.
Staudingers Beiträge zur Chemie wurden 1953 mit der Verleihung des Nobelpreises für Chemie „für seine Entdeckungen auf dem Gebiet der Makromolekularchemie“ offiziell gewürdigt. Diese Auszeichnung war ein Beweis für seinen visionären Ansatz und die weitreichende Bedeutung seiner Arbeit für Wissenschaft und Industrie. Doch auch über seine Nobelpreis-gekrönte Forschung hinaus war Staudinger bekannt für sein Engagement in der Lehre und seine Fähigkeit, die nächste Generation von Chemikern zu inspirieren. Seine Zeit in Freiburg war nicht nur eine Periode intensiver wissenschaftlicher Aktivität, sondern auch der Mentorschaft, in der er viele junge Wissenschaftler auf ihrem Weg begleitete.
Hermann Staudinger verstarb am 8. September 1965, doch sein Vermächtnis lebt in den zahllosen Anwendungen der Polymerchemie im Alltag weiter. Von den Kunststoffen, die in der modernen Gesellschaft allgegenwärtig sind, bis hin zu den synthetischen Fasern in der Bekleidungsindustrie und den Biopolymeren, die für die medizinische Forschung unerlässlich sind, prägt Staudingers Arbeit weiterhin unsere Welt. Seine Beiträge zum Verständnis von Makromolekülen und die Entwicklung synthetischer Methoden wie der Staudinger-Reaktion haben einen bleibenden Eindruck in der Chemie hinterlassen und dafür gesorgt, dass sein Name als einer der großen Pioniere des 20. Jahrhunderts in Erinnerung bleiben wird.
Die organische Chemie verdankt Wolfgang Steglich nicht nur eine der elegantesten Methoden zur Esterbildung, sondern auch zahlreiche Beiträge zur Naturstoffforschung. Geboren 1933 in Kamenz, Sachsen, studierte er Chemie in München, wo er auch promovierte. Nach Stationen an den Universitäten Göttingen und Bonn übernahm er eine Professur an der Universität Bonn und später an der Ludwig-Maximilians-Universität München.
Seine Forschungsschwerpunkte lagen in der Naturstoffchemie, insbesondere in der Isolierung, Strukturaufklärung und Synthese biologisch aktiver Substanzen. Besonders bekannt ist Steglich jedoch für die nach ihm benannte Steglich-Veresterung, bei der Ester unter milden Bedingungen aus Carbonsäuren und Alkoholen hergestellt werden – ermöglicht durch die Aktivierung der Carbonsäure mittels Dicyclohexylcarbodiimid (DCC) und dem Katalysator 4-Dimethylaminopyridin (DMAP).
Diese Methode hat sich in der organischen Synthese etabliert, da sie empfindliche Substrate schont und hohe Ausbeuten liefert – auch bei sterisch anspruchsvollen Alkoholen. Sie ermöglicht es uns, komplexe Zielmoleküle präzise und reproduzierbar herzustellen – ganz im Sinne der Philosophie von Wolfgang Steglich: chemisch elegant und wissenschaftlich durchdacht.
Für seine Verdienste wurde Steglich mit zahlreichen Ehrungen ausgezeichnet, darunter der Emil-Fischer-Preis der Gesellschaft Deutscher Chemiker und die Ehrendoktorwürde mehrerer Universitäten. Seine Reaktion lebt weiter – in unzähligen Laboren weltweit und in der täglichen Arbeit bei ChemCon.
John Kenneth Stille, ein herausragender amerikanischer Chemiker, hinterließ mit seinen bahnbrechenden Forschungen und Beiträgen einen prägenden Einfluss auf die organische Chemie. Geboren im Jahr 1930, widmete Stille sein Leben der wissenschaftlichen Weiterentwicklung, insbesondere in den Bereichen der organischen Synthese und der Polymerchemie. Sein akademischer Werdegang und seine beruflichen Errungenschaften sind ein bleibendes Zeugnis seines Vermächtnisses in der modernen Wissenschaft.
Stille begann sein Chemiestudium an der University of Arizona, wo seine Faszination für die Chemie ihren Ursprung fand. Später promovierte er an der University of Illinois unter der Betreuung von Reynold C. Fuson und spezialisierte sich auf organische Chemie. Diese fundierte Ausbildung rüstete Stille mit dem Wissen und den Fähigkeiten aus, komplexe chemische Herausforderungen zu meistern, und legte den Grundstein für seine späteren Innovationen.
Eine seiner bedeutendsten Leistungen in der Chemie ist die Entwicklung der Stille-Kupplung, einer palladiumkatalysierten Kupplungsreaktion, die die Bildung von Kohlenstoff-Kohlenstoff-Bindungen ermöglicht. Diese Reaktion verbindet ein Organostannan mit einem organischen Halogenid oder Pseudohalogenid. Die Stille-Kupplung ist extrem vielseitig und hat sich als unverzichtbares Werkzeug in der Synthese komplexer organischer Moleküle etabliert, darunter Pharmazeutika, Agrochemikalien und fortschrittliche Materialien. Ihre Fähigkeit, molekulare Architekturen präzise aufzubauen, hat die pharmazeutische Industrie revolutioniert und die Entwicklung wirksamerer und nebenwirkungsärmerer Medikamente ermöglicht.
Neben der Stille-Kupplung leistete John Kenneth Stille bedeutende Beiträge auf dem Gebiet der organischen Polymere. Seine Forschungen konzentrierten sich auf die Synthese und Eigenschaften von Hochleistungspolymeren, die durch ihre herausragende Festigkeit, thermische Stabilität und chemische Widerstandsfähigkeit gekennzeichnet sind. Diese Polymere finden Anwendung in unterschiedlichsten Branchen, von der Luft- und Raumfahrt bis hin zur Elektronik, und verdeutlichen die praktische Bedeutung von Stilles Arbeiten. Durch die Aufklärung der grundlegenden Prinzipien, die die Polymersynthese und -eigenschaften bestimmen, ebnete er den Weg für Innovationen in der Materialwissenschaft, die die moderne Technologie bis heute prägen.
Die Errungenschaften Stilles wirken tiefgreifend in der pharmazeutischen Industrie, wo seine Arbeiten die Synthese komplexer Arzneimittelmoleküle ermöglichten. Die Fähigkeit, komplexe molekulare Strukturen präzise zu konstruieren, ist entscheidend für die Wirkstoffforschung und -entwicklung. Die von ihm entwickelten Methoden haben es Chemikern ermöglicht, Verbindungen zu entwerfen und herzustellen, die Krankheiten effektiver bekämpfen und die Behandlung von Krebs bis hin zu Infektionskrankheiten revolutionieren. Darüber hinaus beeinflussten seine Beiträge zur Polymerchemie die Entwicklung von Arzneimittelabgabesystemen wie bioabbaubaren Polymeren und nanopartikelbasierten Therapien, die für den Fortschritt der personalisierten Medizin von entscheidender Bedeutung sind.
Das Vermächtnis von John Kenneth Stille wird nicht nur durch seine wissenschaftlichen Errungenschaften definiert, sondern auch durch sein Engagement für Bildung und Mentoring. Als Professor an der Colorado State University inspirierte er Generationen von Chemikern, nach Exzellenz in Forschung und Innovation zu streben. Sein Einfluss reicht weit über das Labor hinaus, da seine Entdeckungen weiterhin die Fortschritte in der Chemie und verwandten Gebieten untermauern.
Zusammenfassend verkörpert das Leben und Werk von John Kenneth Stille den tiefgreifenden Einfluss, den eine einzelne Person auf Wissenschaft und Gesellschaft haben kann. Seine wegweisenden Forschungen in der organischen Synthese und Polymerchemie haben nicht nur die Grenzen des Wissens erweitert, sondern auch die Grundlage für praktische Anwendungen gelegt, die der Menschheit zugutekommen. Die Stille-Kupplung und seine Beiträge zur Polymerwissenschaft bleiben Grundpfeiler der modernen Chemie und stellen sicher, dass sein Vermächtnis für kommende Generationen erhalten bleibt.
Adolph Strecker, geboren am 21. Oktober 1822 in Darmstadt, Deutschland, gilt als einer der einflussreichsten Chemiker des 19. Jahrhunderts. Seine Beiträge zur organischen Chemie, insbesondere zur Synthese von Aminosäuren, legten das Fundament für die moderne Biochemie und die pharmazeutische Forschung. Streckers akademische Laufbahn begann mit seinem Studium an der Universität Gießen, wo er von Justus von Liebig, einem der bedeutendsten Chemiker seiner Zeit, betreut wurde. Diese Mentorschaft prägte Streckers wissenschaftlichen Ansatz und förderte eine präzise und innovative Arbeitsweise, die seine Karriere nachhaltig bestimmte.
Am bekanntesten ist Strecker für die Entdeckung der nach ihm benannten Strecker-Synthese. Diese Reaktion, die er 1850 erstmals beschrieb, ist eine bahnbrechende Methode zur Synthese von α-Aminosäuren, den Grundbausteinen von Proteinen. In seinen ursprünglichen Experimenten zeigte Strecker, dass Aldehyde durch Reaktion mit Ammoniak und Cyanwasserstoff α-Aminonitrile bilden können, die anschließend hydrolysiert werden, um α-Aminocarbonsäuren zu erhalten. Dieser einfache, aber elegante Prozess ermöglichte erstmals die Herstellung von Aminosäuren im Labor – eine bemerkenswerte Leistung in einer Zeit, in der die molekularen Grundlagen des Lebens erst ansatzweise verstanden wurden.
Die Bedeutung der Strecker-Synthese reicht weit über ihren historischen Kontext hinaus. In der modernen Chemie wurde die Reaktion an die Anforderungen der pharmazeutischen und biochemischen Forschung angepasst und verfeinert. Eine der bedeutendsten Weiterentwicklungen ist die Entwicklung enantioselektiver Varianten der Strecker-Synthese. Diese Varianten ermöglichen die Herstellung chiraler Aminosäuren mit hoher Stereoselektivität, was für pharmazeutische Anwendungen von entscheidender Bedeutung ist. Viele Medikamente und biologisch aktive Moleküle sind chiral, und oft bestimmt die spezifische Enantiomereigenschaft die Wirksamkeit und Sicherheit eines Arzneimittels. Die Möglichkeit, gezielt das gewünschte Enantiomer mithilfe modifizierter Strecker-Reaktionen herzustellen, ist heute ein zentraler Bestandteil der effizienten und nachhaltigen pharmazeutischen Synthese.
Der Einfluss von Strecker auf die moderne Chemie und die pharmazeutische Industrie ist enorm. Seine Arbeit lieferte nicht nur eine praktische Methode zur Aminosäuresynthese, sondern inspirierte auch nachfolgende Generationen von Chemikern, die Möglichkeiten der organischen Synthese weiter zu erforschen. Die Prinzipien, die der Strecker-Reaktion zugrunde liegen, prägen noch immer die Entwicklung neuer Synthesewege, insbesondere in der Arzneimittelentwicklung. Mithilfe von Methoden, die auf der Strecker-Synthese basieren, hergestellte Aminosäuren werden in der Produktion peptidbasierter Medikamente, von Nahrungsergänzungsmitteln und in zahlreichen biotechnologischen Anwendungen eingesetzt.
Das Vermächtnis von Adolph Strecker ist geprägt von Innovation und nachhaltiger Wirkung. Seine Beiträge zur Chemie schlugen eine Brücke zwischen theoretischem Verständnis und praktischer Anwendung und lieferten Werkzeuge und Erkenntnisse, die heute genauso relevant sind wie im 19. Jahrhundert. Strecker verstarb am 7. November 1871, doch seine Arbeit wirkt bis heute nach und prägt die Felder der organischen Chemie und der pharmazeutischen Wissenschaft auf eine Weise, die er sich kaum hätte vorstellen können.
Akira Suzuki wurde am 12. September 1930 in Mukawa, Präfektur Hokkaidō Japan geboren. 1959 promovierte er an der Universität Hokkaidō und wurde zwei Jahre später Assistenzprofessor dort. Von 1963 bis 1965 arbeitete er unter Nobelpreisträger Herbert Charles Brown an der Purdue University als Postdoktorand. Ab 1973 war er als Professor an japanischen Universitäten tätig. Zuerst in der Abteilung der Angewandten Chemie der Universität Hokkaidō, dann an der Universität Okayama und 1995 an der Kurashiki-Universität. Er hatte außerdem Gastprofessuren an der University of Wales und an der Purdue University.
Er forschte auf dem Gebiet der organischen Chemie, genauer untersuchte er Organoborverbindungen und deren Anwendungen in Synthese und Organometallchemie. Mit Brown arbeitete er an Hydroborierung und organischen Radikalen auf Organoboran-Basis. Er führte Organoborverbindungen als Carbanionen in die chemische Synthese ein. Später galt sein Interesse der Palladium-katalysierten Kreuzkupplung von Organoborverbindungen wo er die Suzuki-Kupplung entdeckte.
Für diese Entdeckung wurde ihm 2010 zusammen mit Ei-Ichi Negishi und Richard F. Heck der Nobelpreis für Chemie verliehen.
Im Jahr 2023 ging der Nobelpreis der Chemie an Moungi Bawendi, Alexei Iwanowitsch Jekimow und Louis Brus. Sie entdeckten und entwickelten Quantenpunkte. Diese sind für verschiedene Anwendungen von Interesse.
Zum Beispiel:
- Markerfarbstoffe
- LED’s
- Quantenpunktlaser
- Quantencomputing
- u.v.m.
Daniel Swern war ein renommierter amerikanischer Chemiker, der von 1916 bis 1982 lebte. Er machte sich insbesondere einen Namen durch seine bedeutenden Beiträge zur Organischen Chemie. Eine seiner herausragenden Leistungen ist die Entwicklung der nach ihm benannten Swern-Oxidation. Diese Namensreaktion, auch als Swern-Umlagerung bekannt, ermöglicht die milde und selektive Oxidation sekundärer Alkohole zu Ketonen, ohne dabei primäre Alkohole zu beeinträchtigen. Die Swern-Oxidation wird weltweit in der organischen Synthese eingesetzt und hat sich als äußerst nützliches Werkzeug für die Umwandlung von Alkoholen in Ketone erwiesen, ohne dabei auf stark oxiderende Bedingungen zurückgreifen zu müssen.
Daniel Swerns Hingabe zur Forschung und seine innovativen Beiträge in der Organischen Chemie haben seinen Einfluss über seinen Tod hinaus fortbestehen lassen. Die Swern-Oxidation ist zu einem festen Bestandteil im Arsenal von Organikern geworden, die komplexe Moleküle synthetisieren und dabei die empfindlichen Strukturen schonend manipulieren möchten. Swerns Vermächtnis lebt somit nicht nur in seiner eigenen akademischen Laufbahn weiter, sondern auch in der täglichen Arbeit von Chemikern weltweit, die von seinen Entwicklungen profitieren.
Die Swern Reaktion findet in folgenden Gebieten Anwendung:
- Pharmazeutische Industrie: In der Herstellung von pharmazeutischen Wirkstoffen können Alkohole durch die Swern-Oxidation in Keton-Strukturen umgewandelt werden. Dies kann ein entscheidender Schritt in der Synthese von Arzneimitteln sein.
- Feinchemikalienproduktion: In der Produktion von Feinchemikalien, die in verschiedenen Industriezweigen verwendet werden, kann die Swern-Reaktion eingesetzt werden, um spezifische Keton-Strukturen zu erzeugen.
- Aromachemikalien: In der Aromachemikalien-Industrie, insbesondere bei der Herstellung von Duftstoffen und Aromastoffen, kann die Swern-Oxidation eine Rolle bei der Synthese bestimmter Moleküle spielen.
- Materialwissenschaften: In einigen Fällen wird die Swern-Oxidation auch in der Herstellung von Polymeren und anderen Materialien genutzt, in denen spezifische Ketongruppen eingeführt werden müssen.
Frederick Nye Tebbe...
... war ein metallorganischer Chemiker, der das so genannte Tebbe-Reagenz veröffentlichte, mit dem man eine Methylengruppe anstelle einer Carbonylfunktion einführen kann.
Tebbe wurde in Oakland, Kalifornien, geboren. Er studierte Chemie und erhielt einen Bachelor-Abschluss an der Pennsylvania State University.
Nach dem Chemiestudium ging er für ein Jahr an die Montana State University und studierte Psychologie und Philosophie. Im Jahr 1965 wurde er von der zentralen Forschungsabteilung von DuPont eingestellt, wo er das Tebbe-Reagenz entwickelte, das von Robert Grubbs (Nobelpreis 2005) nach ihm benannt wurde.
Alfred Einhorn: Ein Pionier der Chemie und die Tscherniak-Einhorn-Reaktion
In der Geschichte der Chemie gibt es Namen, die durch ihre bahnbrechenden Entdeckungen und Beiträge zur Wissenschaft unvergessen bleiben. Alfred Einhorn gehört zweifellos zu diesen herausragenden Persönlichkeiten. Seine Arbeit hat nicht nur das Feld der organischen Chemie bereichert, sondern auch praktische Anwendungen in der Medizin und Pharmazie maßgeblich beeinflusst. In diesem Beitrag widmen wir uns dem Leben und Wirken von Alfred Einhorn sowie seiner berühmten Tscherniak-Einhorn-Reaktion.
Leben und akademische Laufbahn
Alfred Einhorn wurde am 27. Februar 1856 in Hamburg geboren. Seine akademische Reise in die Welt der Chemie begann an der Universität München, wo er unter der Leitung von Adolf von Baeyer studierte, einem der bedeutendsten Chemiker seiner Zeit. Einhorns wissenschaftliche Neugier und sein tiefes Verständnis für organische Verbindungen führten zu zahlreichen Entdeckungen, die seine Karriere prägten.
Einflussreiche Beiträge zur Chemie
Einhorns Forschungsinteressen waren vielfältig, aber besonders hervorzuheben ist seine Arbeit auf dem Gebiet der Lokalanästhetika. Sein wohl bekanntester Beitrag zur Chemie und Medizin ist die Synthese von Procain im Jahr 1905, besser bekannt unter dem Handelsnamen Novocain. Diese Entdeckung revolutionierte die chirurgische Medizin, indem sie eine wirksame und weniger toxische Alternative zu den damals verwendeten Lokalanästhetika bot.
Die Tscherniak-Einhorn-Reaktion
Eine weitere bedeutende Leistung Einhorns ist die Entwicklung der Tscherniak-Einhorn-Reaktion, benannt nach ihm und seinem Kollegen Tscherniak. Diese chemische Reaktion erweiterte das Verständnis der Synthese organischer Verbindungen und hatte bedeutende Auswirkungen auf die organische Chemie. Die Tscherniak-Einhorn-Reaktion ermöglicht die Synthese von α-Hydroxyphosphonaten, die als Schlüsselintermediate in der organischen Synthese und bei der Entwicklung von Pharmazeutika eine wichtige Rolle spielen.
Zusammenarbeit und Einfluss
Alfred Einhorns Arbeit war geprägt von Zusammenarbeit mit anderen Wissenschaftlern und von seinem Bestreben, die Grenzen des damaligen chemischen Wissens zu erweitern. Sein Einfluss auf nachfolgende Generationen von Chemikern und seine Beiträge zur organischen Synthese und pharmazeutischen Chemie sind unermesslich. Seine Forschungen legten den Grundstein für moderne Anästhesiemethoden und verbesserten die Lebensqualität von Millionen von Patienten weltweit.
Vermächtnis und moderne Wissenschaft
Das Vermächtnis von Alfred Einhorn reicht weit über seine Lebenszeit hinaus. Die von ihm entwickelten Methoden und Verbindungen sind bis heute Grundlage für wissenschaftliche Forschung und medizinische Praxis. Die Tscherniak-Einhorn-Reaktion und die Synthese von Novocain sind nur zwei Beispiele für Einhorns bahnbrechende Arbeit, die die Chemie und die Medizin nachhaltig verändert haben.
Fazit
Alfred Einhorn war ein visionärer Wissenschaftler, dessen Neugier und Innovationsgeist die Grenzen des Verständnisses in der Chemie erweiterten. Seine Entdeckungen, insbesondere die Tscherniak-Einhorn-Reaktion und die Synthese von Novocain, haben ihn zu einer Schlüsselfigur in der Entwicklung der modernen Chemie und Pharmazie gemacht. Sein Erbe lebt in jeder Anwendung seiner Forschung weiter, ein bleibendes Zeugnis für die Kraft der Wissenschaft, das menschliche Leben zu verbessern.
Barry Trost ist ein renommierter amerikanischer Chemiker, dessen Arbeiten die organische Synthese nachhaltig geprägt haben. Geboren 1941, absolvierte er sein Studium an der University of Pennsylvania und promovierte anschließend am Massachusetts Institute of Technology (MIT). Nach Stationen an der University of Wisconsin-Madison wechselte er an die Stanford University, wo er bis heute tätig ist.
Trost ist bekannt für seine Arbeiten zur atomökonomischen Synthese, bei der chemische Prozesse so gestaltet werden, dass möglichst wenig Abfall entsteht. Eine seiner bedeutendsten Entdeckungen ist die nach ihm und Tamejiro Tsuji benannte Tsuji-Trost-Reaktion. Diese Palladium-katalysierte Allylierung ermöglicht die gezielte Einführung von funktionellen Gruppen in organische Moleküle und wird insbesondere für die Synthese von Naturstoffen, Pharmawirkstoffen und komplexen organischen Strukturen genutzt. Sie hat moderne Synthesestrategien revolutioniert, da sie hohe Selektivität und Effizienz bietet.
Im Laufe seiner Karriere erhielt Trost zahlreiche Auszeichnungen, darunter die renommierten ACS Awards in organischer Chemie sowie den Wolf-Preis. Seine Arbeiten haben nicht nur die Forschung geprägt, sondern finden auch in der industriellen Synthese Anwendung.
ChemCon setzt die Tsuji-Trost-Reaktion in der kundenspezifischen Synthese ein, um maßgeschneiderte organische Verbindungen für pharmazeutische und biotechnologische Anwendungen herzustellen. Durch diese effiziente Methode können hochreine Zwischenprodukte mit hoher Selektivität und atomökonomischem Ansatz synthetisiert werden, was zur Nachhaltigkeit und Qualitätssicherung beiträgt.
Ivar Ugi, geboren 1930 in Kuressaare, Estland, war ein bedeutender Chemiker, dessen Arbeit die organische Synthese revolutionierte. Nach dem Zweiten Weltkrieg emigrierte er nach Deutschland, wo er seine akademische Laufbahn begann. Er studierte Chemie an der Universität Tübingen und promovierte 1954 unter der Leitung des berühmten Chemikers Rolf Huisgen. In den 1960er Jahren entwickelte Ugi die nach ihm benannte Ugi-Reaktion, eine Mehrkomponentenreaktion, die bis heute einen erheblichen Einfluss auf die chemische Forschung und Industrie hat.
Ugi war in seiner akademischen Karriere äußerst erfolgreich und hatte mehrere Professuren inne, unter anderem in München. Er arbeitete an renommierten Forschungsinstituten und leistete bedeutende Beiträge zur Chemie, insbesondere im Bereich der organischen Synthese. Seine Forschung führte zu zahlreichen Veröffentlichungen und Patenten, die die Art und Weise, wie Chemiker Moleküle und Wirkstoffe synthetisieren, maßgeblich veränderten.
Die Ugi-Reaktion ist eine der bekanntesten Mehrkomponentenreaktionen, bei der ein Keton oder Aldehyd, ein Amin, ein Isonitril und eine Carbonsäure in einer einzigen Reaktion zu einem Bis-Amid umgesetzt werden. Diese Reaktion ist nicht nur effizient, sondern ermöglicht auch eine große Variabilität bei der Auswahl der Reagenzien, was sie zu einem wertvollen Werkzeug in der pharmazeutischen Chemie macht. Die schnelle und einfache Durchführung der Ugi-Reaktion hat sie zu einer bevorzugten Methode in der Wirkstoffentwicklung gemacht.
Ein herausragendes Beispiel für die Bedeutung der Ugi-Reaktion ist ihre Rolle bei der Synthese von Indinavir, einem Medikament zur Behandlung von HIV. Indinavir ist ein Protease-Inhibitor, der bei der HIV-Therapie eingesetzt wird, um die Vermehrung des Virus zu blockieren. Die Ugi-Reaktion ermöglichte die effiziente und skalierbare Synthese von Indinavir und trug so entscheidend zur Entwicklung dieses lebensrettenden Medikaments bei.
Die Bedeutung von Ugis Arbeit in der HIV-Therapie kann kaum überschätzt werden. Durch die Anwendung der Ugi-Reaktion konnten komplexe Wirkstoffe wie Indinavir in kürzerer Zeit und mit höherer Effizienz synthetisiert werden. Dies trug dazu bei, die Behandlungsmöglichkeiten für Millionen von HIV-Patienten weltweit zu verbessern. Ivar Ugi hat mit seiner Entdeckung nicht nur die Chemie weitergebracht, sondern auch einen bleibenden Beitrag zur medizinischen Forschung und zur Bekämpfung einer der schwerwiegendsten Epidemien unserer Zeit geleistet.
Fritz Ullmann war ein Deutscher Chemiker.
Er studierte an der Universität in Genf, wo er 1895 promoviert wurde. An der Technische Hochschule Berlin lehrte er von 1905 bis 1913 als Privatdozent und von 1922 bis 1925 als assoziierter Professor.
Von 1914 bis 1922, veröffentlichte er die erste Auflage der Encyclopedie der Technischen Chemie in 12 Bänden ein Standardwerk, das seit dieser Zeit immer wieder Aktualisierung erfährt.
Er entwickelte einige wichtige Synthese Methoden wie die Synthese von Diarylaminen, Synthese von Carbazolen und die hier vorgestellte Ullmann Reaktion zur Herstellung von Biarylen.
Franz Varrentrapp war ein deutscher Chemiker des 19. Jahrhunderts, dessen Beiträge zur analytischen Chemie heute vor allem durch die nach ihm benannte Varrentrapp-Reaktion bekannt sind. Er wurde am 18. November 1815 in Braunschweig geboren und studierte Naturwissenschaften, unter anderem in Göttingen. Später arbeitete er eng mit Justus von Liebig zusammen, einem der bedeutendsten Chemiker seiner Zeit, was seine wissenschaftliche Entwicklung maßgeblich prägte. Varrentrapp widmete sich insbesondere der Entwicklung von Methoden zur Bestimmung chemischer Elemente in organischen Verbindungen, was in einer Zeit der rasanten Weiterentwicklung der organischen Chemie von zentraler Bedeutung war. Seine Arbeit trug wesentlich zur Standardisierung analytischer Verfahren bei und ebnete den Weg für moderne Methoden der Elementaranalyse.
Die Varrentrapp-Reaktion ist eine klassische Methode zum Nachweis und zur quantitativen Bestimmung von Schwefel in organischen Verbindungen. Dabei wird die organische Verbindung mit Natrium erhitzt, wodurch Schwefel in Form von Natriumsulfid freigesetzt wird. Dieses kann im Anschluss durch Fällung als Blei(II)-sulfid nachgewiesen werden. Obwohl die Methode heute weitgehend durch moderne Analyseverfahren ersetzt wurde, bleibt sie ein historisch bedeutsames Beispiel für die frühen Entwicklungen der quantitativen Elementaranalyse. ChemCon greift im Rahmen der Methodenentwicklung und zur Validierung analytischer Prozesse auch heute noch gelegentlich auf klassische Verfahren wie die Varrentrapp-Reaktion zurück, insbesondere wenn es darum geht, robuste und nachvollziehbare Nachweise für regulatorisch relevante Elemente wie Schwefel zu liefern.
Anton Vilsmeier war ein deutscher Chemiker, der durch die nach ihm benannte Vilsmeier-Haack-Reaktion einen bedeutenden Beitrag zur organischen Chemie leistete. Geboren am 12. Juni 1894 in Burgweinting, heute ein Stadtteil von Regensburg, zeigte Vilsmeier früh Interesse an den Naturwissenschaften. Nach dem Abitur begann er 1920 ein Chemiestudium an der Universität München und setzte es ab 1922 an der Universität Erlangen fort. Dort promovierte er 1924 bei Otto Fischer mit einer Arbeit über Gamma-Chlor-Iso-Chinocyanine aus Methyl-(Aethyl-)Acetanilid und Phosphoroxychlorid.
Während seiner Zeit in Erlangen arbeitete Vilsmeier eng mit Albrecht Haack zusammen. Gemeinsam entwickelten sie 1927 die Vilsmeier-Haack-Reaktion, eine Methode zur Formylierung von aromatischen und heterocyclischen Verbindungen mittels Dimethylformamid (DMF) und Phosphoroxychlorid, die zu Aryl- und Heteroarylaldehyden führt. Diese Reaktion erwies sich als äußerst effizient und vielseitig und fand schnell breite Anwendung in der Synthese von Zwischenprodukten für Farbstoffe und Arzneimittel.
1927 trat Vilsmeier eine Position bei der BASF in Ludwigshafen an, wo er bis zu seiner Pensionierung 1959 tätig war. Während seiner industriellen Karriere konzentrierte er sich auf die Entwicklung von Küpenfarbstoffen der Indanthren-Reihe und trug maßgeblich zur Weiterentwicklung der Farbstoffchemie bei. Seine Arbeiten beeinflussten nicht nur die akademische Welt, sondern auch die chemische Industrie nachhaltig. Die Möglichkeit, Aromaten gezielt zu formylieren, ermöglichte die Herstellung komplexer Moleküle, die als Grundbausteine in der pharmazeutischen Wirkstoffentwicklung dienen. Viele pharmazeutische Wirkstoffe basieren auf Arylaldehyden, die durch die Vilsmeier-Haack-Reaktion effizient hergestellt werden können.
Bei ChemCon wird diese historische Reaktion mit modernster Technologie kombiniert, um höchste Reinheit und Effizienz in der Produktion zu gewährleisten. Als führendes Unternehmen im Bereich der Auftragsynthese nutzt ChemCon die Vilsmeier-Haack-Reaktion, um maßgeschneiderte Moleküle nach den individuellen Anforderungen unserer Kunden zu entwickeln. Diese Flexibilität ermöglicht es, innovative Wirkstoffe und Zwischenprodukte zu synthetisieren, die den strengen GMP-Richtlinien entsprechen. Durch die Anwendung dieser klassischen, aber hochaktuellen Synthesemethode kann ChemCon komplexe organische Verbindungen effizient herstellen und so zur Weiterentwicklung der pharmazeutischen Industrie beitragen. Anton Vilsmeiers Erbe lebt in der modernen chemischen Synthese weiter und zeigt, wie zeitlos seine wissenschaftliche Leistung ist.
Julius von Braun war ein deutscher Chemiker, der am 26. Juli 1875 in Warschau geboren wurde und am 8. Januar 1939 in Heidelberg verstarb. Nachdem er 1893 seine Reifeprüfung am humanistischen Gymnasium in Warschau abgelegt hatte, studierte er Chemie an der Universität Göttingen, der Königlich Technischen Hochschule Charlottenburg und der Universität München. Im Jahr 1898 promovierte er unter dem Nobelpreistärger Otto Wallach an der Universität Göttingen.
Braun arbeitete als Assistent am Chemischen Institut in Göttingen und wurde 1902 Privatdozent. 1909 wurde er Außerordentlicher Professor an der Universität Breslau und später Professor an der Landwirtschaftlichen Hochschule Berlin. 1921 wechselte er als ordentlicher Professor für Chemie an die Universität Frankfurt am Main.
Braun erforschte die Reaktionen zahlreicher Alkaloide und synthetisierte organische Verbindungen. Er entdeckte auch die Rosenmund-von-Braun-Reaktion und die Von-Braun-Reaktion. Letztere ist auch als Von-Braun-Amid-Abbau bekannt und eine Namensreaktion der organischen Chemie. Bei dieser Synthese entstehen Halogenalkane und Nitrile.
Heute haben Halogenalkane eine Vielzahl von Anwendungen, darunter als Lösungsmittel, Kühlmittel, Treibmittel, Flammschutzmittel und in der Medizin. Die Verwendung von Halogenalkanen als Treibmittel in der Medizin ist jedoch umstritten, da sie zur Zerstörung der Ozonschicht beitragen können.
Georg Friedrich Karl Wittig:
Wittig war ein deutscher Chemiker und Nobelpreisträger. Aufgrund seines familiären Hintergrunds war er künstlerisch sehr begabt. Er spielte Klavier, komponierte und malte sehr gut. Doch seine Liebe galt der Chemie. Obwohl er mitten in seinem Chemiestudium eingezogen wurde und in Kriegsgefangenschaft geriet, setzte er sein Studium fort, sobald er frei war.
Mittels der Wittig-Reaktion können Kohlenstoff-Kohlenstoff Doppelbindungen geknüpft werden. Dabei kommt eine Carbonylverbindung und ein Phosphonium Ylid zum Einsatz, wobei der Carbonly-Sauerstoff gegen den Kohlenstoff substituiert wird.
Karl Ziegler war ein deutscher Chemiker, der für seine Beiträge zur Polymerchemie, der metallorganischen Chemie und der homogenen Übergangsmetall-Katalyse bekannt ist. Er wurde 1898 in Helsa geboren und studierte Chemie an der Universität Marburg, wo er 1920 promovierte. Er arbeitete zunächst bei der I.G. Farben Industrie AG, bevor er eine akademische Laufbahn einschlug. Er war Professor an den Universitäten Frankfurt, Heidelberg und Tübingen, bevor er 1943 die Leitung des Max-Planck-Instituts für Kohlenforschung in Mülheim an der Ruhr übernahm.
Zu seinen wichtigsten wissenschaftlichen Errungenschaften gehört die Entdeckung der Ziegler-Natta-Katalyse, die es ermöglicht, Polymere mit einer präzisen Molekularstruktur herzustellen. Diese Polymere haben verbesserte Eigenschaften und finden vielfältige Anwendungen in der Kunststoffindustrie. Ziegler erfand auch das Ziegler-Verfahren zur Herstellung von Fettalkoholen aus Ethen und Triethylaluminium, die als Rohstoffe für biologisch abbaubare Waschmittel dienen. Außerdem erforschte er freie Radikale, alkaliorganische Verbindungen, Ringschlussreaktionen, Naturstoffe und elektrochemische Phänomene.
Für seine herausragenden Leistungen wurde Ziegler mit zahlreichen Ehrungen ausgezeichnet, darunter der Nobelpreis für Chemie im Jahr 1963, den er sich mit Giulio Natta teilte. Er war auch Mitbegründer und erster Präsident der Gesellschaft Deutscher Chemiker (GDCh) und Ehrenbürger der Stadt Mülheim. Er stiftete einen Großteil seines Vermögens für die Förderung der chemischen Forschung und hinterließ eine bedeutende Kunstsammlung. Er starb 1973 im Alter von 74 Jahren.
Ludwig Wolff: Eine tragende Säule in der organischen Chemie und pharmazeutischen Innovation
Unter den vielen Namen, die in den Geschichtsbüchern der Chemie verewigt sind, sticht Ludwig Wolff besonders hervor. Als deutscher Chemiker hat sein Schaffen weitreichende Wellen geschlagen, die nicht nur akademische Kreise beeindruckt, sondern auch die pharmazeutische Industrie maßgeblich geformt haben. Geboren im ausgehenden 19. Jahrhundert, begab sich Wolff auf eine Entdeckungsreise in die Tiefen der organischen Chemie. Er entdeckte Reaktionen und Verfahren, die seinen Namen tragen und bis heute von immenser Bedeutung sind.
Wolffs akademischer Werdegang zeugt von seiner herausragenden Brillanz und seinem unermüdlichen Engagement. Er war für seinen strengen Forschungsansatz und seine unstillbare Neugier bekannt, die ihn dazu antrieben, das komplexe Zusammenspiel von Atomen und Molekülen zu erforschen. Seine Pionierarbeit legte den Grundstein, auf dem zukünftige Generationen von Chemikern aufbauen konnten. Von seinen zahlreichen Beiträgen ragt besonders die Wolff-Umlagerung heraus, ein glänzendes Beispiel seines Erfindungsgeistes.
Die Wolff-Umlagerung, eine chemische Reaktion, die die Umordnung von α-Diazoketonen zu Keten umfasst, gilt als Eckstein in der synthetischen organischen Chemie. Dieser Prozess hat sich als unerlässliches Werkzeug für Chemiker erwiesen, da er die Synthese komplexer Moleküle aus einfacheren Vorstufen ermöglicht. Die Tatsache, dass diese Entdeckung heute in Bereichen Anwendung findet, die weit über Wolffs ursprüngliche Vorstellungen hinausgehen – besonders in der pharmazeutischen Industrie –, spricht Bände über seine visionäre Denkweise.
In der heutigen pharmazeutischen Forschung spielt die Wolff-Umlagerung eine Schlüsselrolle bei der Synthese verschiedenster Verbindungen, darunter Antibiotika und entzündungshemmende Mittel. Ihre Effizienz in der Erzeugung von Keten, die leicht in eine Vielzahl funktionaler Gruppen umgewandelt werden können, macht sie zu einem unverzichtbaren Instrument in der Entwicklung neuer Medikamente. Die durch diese Umlagerung gebotene Flexibilität und Vielseitigkeit haben es Forschern ermöglicht, innovative und zielgerichtete Therapien zu entwickeln, die die Patientenversorgung verbessern und zur Fortentwicklung der medizinischen Wissenschaft beitragen.
Darüber hinaus geht Wolffs Einfluss weit über seine eigenen Entdeckungen hinaus. Seine Leidenschaft für die Forschung und sein innovativer Geist haben Generationen von Chemikern inspiriert. Er verkörpert das Streben nach Erkenntnis und die Ausdauer, die notwendig sind, um nicht nur intelligent, sondern auch kreativ und hartnäckig zu sein.
Das Erbe Ludwig Wolffs lebt nicht nur in Lehrbüchern fort, sondern auch in den Laboren, wo seine Arbeit weiterhin als Inspiration für Neuerungen dient. Während sich die pharmazeutische Industrie weiterentwickelt, bleiben die von ihm entwickelten Prinzipien und Prozesse ein zentraler Bestandteil der Arzneimittelentwicklung. Seine Beiträge bilden das Fundament für neue Entdeckungen und zeigen die nachhaltige Wirkung seiner Arbeit auf die Gesundheit und das Wohl der Gesellschaft auf.
Abschließend lässt sich sagen, dass Ludwig Wolffs Leben und wissenschaftliche Errungenschaften den tiefgreifenden Einfluss illustrieren, den eine Person auf die Welt haben kann. Die Wolff-Umlagerung steht als Zeugnis seines Genies, ein Geschenk an die Chemie und Medizin, das die pharmazeutische Industrie in neue Dimensionen geführt hat. Mit Blick auf die Zukunft dient Wolffs Vermächtnis als Fundament und Leitstern, der die kontinuierlichen Bemühungen leitet, die Geheimnisse der Chemie zu entschlüsseln und zum Wohle der Menschheit zu nutzen.
Charles Adolphe Wurtz, auch als Karl Adolph Wurtz bekannt, war ein renommierter französischer Chemiker und Arzt, der am 26. November 1817 in Straßburg zur Welt kam und am 12. Mai 1884 in Paris verstarb. Sein wissenschaftlicher Fokus lag auf der Chemie der Kohlenwasserstoffe und organischen Stickstoffverbindungen.
Wurtz wurde als Sohn von Jean Jacques Wurtz, einem evangelischen Pfarrer, in Straßburg und Wolfisheim geboren, wo er auch seine Kindheit verbrachte. Nach dem Abschluss des evangelischen Gymnasiums in Straßburg im Jahr 1834, begann er mit der Unterstützung seines Vaters ein Medizinstudium. Seine besondere Neigung zur klinischen Chemie führte dazu, dass er 1839 zum Chef des travaux chimiques an der Medizinischen Fakultät in Straßburg ernannt wurde.
Wurtz ist bekannt für die Synthese von Ethylamin und die Entdeckung von Glycol und Phosphoroxychlorid. Zusammen mit Rudolph Fittig wurde die Wurtz-Fittig-Synthese benannt, ein Verfahren zur Herstellung von Kohlenwasserstoffen aus Halogenalkanen durch Einwirkung von Alkalimetallen.
Nach einem Studienjahr bei Justus von Liebig in Gießen kehrte er nach Paris zurück und arbeitete im Labor von Jean-Baptiste Dumas. Im Jahr 1845 wurde er Assistent von Dumas an der École de Médicine de Paris und begann vier Jahre später, Vorlesungen über organische Chemie zu halten.
Trotz der bescheidenen Ausstattung seines Labors an der École de Médicine de Paris eröffnete er 1850 ein eigenes privates Laboratorium in der Rue Garenciere. Im selben Jahr wurde er Professor für Chemie am neu gegründeten Institut Agronomique in Versailles, das jedoch bereits 1852 wieder geschlossen wurde.
Im Jahr 1853 übernahm er den Lehrstuhl für Organische Chemie an der Medizinischen Fakultät, der durch den Rücktritt von J.B.A. Dumas frei geworden war. Im Jahr 1866 wurde er Dekan der Fakultät für Medizin. Er behielt den Titel eines Ehren-Dekans, als er 1875 aus dem Amt ausschied.
Wurtz war Ehrenmitglied fast aller wissenschaftlichen Gesellschaften in Europa. Er war Mitbegründer der Société Chimique de France (1858), war dort erster Sekretär und dreimal Präsident. Seine Arbeit und sein Einfluss auf die Chemie sind bis heute spürbar, insbesondere durch die nach ihm benannte Wurtz-Reaktion.
Das von ihm entdeckte Ethylamin wird in der Herstellung von vielen Herbiziden, Pestiziden und der Herstellung von Gummi verwendet. Das Ethylenglycol wird in Frostschutzmitteln und der Herstellung von Polyester Fasern verwendet.
Masaru Yamaguchi ist eine herausragende Persönlichkeit im Bereich der organischen Chemie, dessen bahnbrechende Arbeiten einen bleibenden Einfluss auf die wissenschaftliche Gemeinschaft ausgeübt haben. Als Professor an der Universität Kyoto hat Yamaguchi mit seinen innovativen Ansätzen zur Synthese den Weg für zahlreiche Fortschritte in der chemischen Forschung geebnet.
Eine der bekanntesten Beiträge von Yamaguchi ist die Entwicklung der Yamaguchi-Cyclisierung, eine Methode, die die Synthese von makrozyklischen Laktone revolutioniert hat. Diese Reaktion umfasst die Bildung von makrozyklischen Ringen aus Hydroxycarbonsäuren unter Verwendung von Yamaguchis einzigartigen Reagenzien, wie 2,4,6-Trichlorbenzoylchlorid (TCBC) und 4-Dimethylaminopyridin (DMAP). Das Verfahren zeichnet sich durch seine Effizienz und hohe Ausbeute aus und ermöglicht die Herstellung großer, komplexer Ringstrukturen, die für verschiedene Naturstoffe und pharmazeutische Produkte von entscheidender Bedeutung sind.
Die Yamaguchi-Cyclisierung ist insbesondere bei der Synthese von Makroliden von Bedeutung, einer Klasse von Naturstoffen mit starken biologischen Aktivitäten, darunter Antibiotika- und Antikrebseigenschaften. Durch die Vereinfachung der Bildung dieser komplizierten Strukturen ist Yamaguchis Methode zu einem festen Bestandteil in organischen Syntheselabors weltweit geworden.
Die Beiträge von Masaru Yamaguchi gehen über seine benannte Cyclisierung hinaus. Seine Forschung hat die Grundlage für Fortschritte in der Katalyse, der grünen Chemie und der Arzneimittelentwicklung gelegt. Yamaguchis Arbeiten haben die Entwicklung neuer katalytischer Prozesse inspiriert, die die Effizienz und Selektivität chemischer Reaktionen verbessern. Mit einem Schwerpunkt auf Nachhaltigkeit beinhalten seine Methoden oft mildere Bedingungen und weniger Nebenprodukte, was den Prinzipien der grünen Chemie entspricht. Darüber hinaus hat die Fähigkeit, komplexe Moleküle effizient zu synthetisieren, die Entdeckung und Produktion neuer pharmazeutischer Produkte, insbesondere solcher, die makrozyklische Strukturen enthalten, beschleunigt.
Heute zeigt sich der Einfluss von Masaru Yamaguchi in der fortgesetzten Erforschung von Cyclisierungstechniken und der anhaltenden Suche nach nachhaltigeren und effizienteren chemischen Prozessen. Forscher bauen auf seiner Pionierarbeit auf und streben danach, die Grenzen des Möglichen in der organischen Synthese zu erweitern. Yamaguchis Engagement für Innovation und Exzellenz in der Chemie dient als bleibende Inspiration für Chemiker weltweit und stellt sicher, dass sein Erbe das Fachgebiet noch lange prägen wird.
Theodor Zincke wurde am 19. Mai 1843 in Uelzen geboren und war ein einflussreicher deutscher Chemiker, dessen Arbeiten und Entdeckungen einen bedeutenden Einfluss auf die moderne Chemie haben. Zincke studierte an der Universität Göttingen, wo er 1865 promovierte. Anschließend arbeitete er bei verschiedenen Chemikern in Deutschland und Frankreich, darunter Hermann Kolbe und Charles-Adolphe Wurtz, was ihm half, seine Kenntnisse und Fähigkeiten in der organischen Chemie zu vertiefen.
Seine akademische Laufbahn begann an der Universität Marburg, wo er 1872 zum Professor für Chemie ernannt wurde. Später, 1875, wechselte er an die Universität Bonn, wo er bis zu seiner Emeritierung im Jahr 1913 tätig war. In Bonn leitete er das chemische Institut und führte zahlreiche wegweisende Forschungen durch.
Eine seiner bedeutendsten wissenschaftlichen Errungenschaften war die Entwicklung der nach ihm benannten Zincke-Reaktion. Diese Reaktion, bei der Pyridine in Pyridinium-Salze umgewandelt werden, war ein wichtiger Beitrag zur organischen Synthese und fand breite Anwendung in der Erforschung von Heterocyclen. Darüber hinaus erforschte Zincke die Chemie der Chinone und Nitroverbindungen, was ebenfalls zu wichtigen Erkenntnissen in der organischen Chemie führte.
Zinckes Arbeit hatte einen nachhaltigen Einfluss auf die chemische Forschung und Lehre. Seine Studien zur Struktur und Reaktivität organischer Moleküle legten den Grundstein für viele moderne Entwicklungen in der Chemie. Insbesondere seine Arbeiten über Pyridine und die von ihm entwickelten Reaktionen sind nach wie vor relevant und werden in der organischen Synthese und der pharmazeutischen Chemie verwendet.
Theodor Zincke war auch ein engagierter Lehrer und Mentor für viele junge Chemiker. Unter seiner Anleitung wurden zahlreiche Doktorarbeiten angefertigt, und viele seiner Schüler machten selbst bedeutende Karrieren in der Chemie. Zinckes Einfluss auf die heutige Wissenschaft ist daher nicht nur in seinen eigenen Entdeckungen, sondern auch in der Ausbildung und Inspiration der nächsten Generation von Chemikern zu sehen.
Er starb am 17. März 1928, aber sein Erbe lebt weiter. Die von ihm entwickelten Reaktionen und Methoden sind fester Bestandteil des chemischen Wissens und werden weiterhin in Forschung und Industrie angewendet. Zincke bleibt ein herausragendes Beispiel für einen Wissenschaftler, dessen Arbeit und Einfluss weit über seine eigene Lebenszeit hinausreichen.